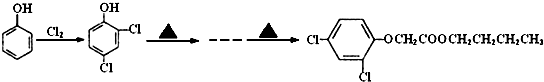题目内容
在相同温度时,100mL 0.01mol?L-1的醋酸溶液与10mL 0.1mol?L-1的醋酸溶液相比较,下列数据中,前者大于后者的是( )
①H+的物质的量 ②电离程度
③中和时所需氢氧化钠的量 ④醋酸的物质的量.
①H+的物质的量 ②电离程度
③中和时所需氢氧化钠的量 ④醋酸的物质的量.
| A、①② | B、②③ | C、①④ | D、②④ |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:在相同温度时,100mL 0.01mol?L-1的醋酸溶液与10mL0.1mol?L-1的醋酸溶液中溶质都为0.001mol,醋酸为弱电解质,浓度不同,电离程度不同,浓度越大,电离程度越小,以此解答该题.
解答:
解:①醋酸为弱电解质,浓度越大,电离程度越小,两种溶液溶质都为0.001mol,则100mL 0.01mol?L-1的醋酸溶液与10mL0.1mol?L-1的醋酸溶液相比较,H+的物质的量前者大,故①正确;
②醋酸为弱电解质,浓度越大,电离程度越小,电离程度0.01mol?L-1的醋酸大,故②正确;
③由于溶质n(CH3COOH)都为0.001mol,中和时所需NaOH的量应相同,故③错误;
④0.01mol?L-1的醋酸电离程度大,则溶液中CH3COOH分子的物质的量小,故④错误.
故选A.
②醋酸为弱电解质,浓度越大,电离程度越小,电离程度0.01mol?L-1的醋酸大,故②正确;
③由于溶质n(CH3COOH)都为0.001mol,中和时所需NaOH的量应相同,故③错误;
④0.01mol?L-1的醋酸电离程度大,则溶液中CH3COOH分子的物质的量小,故④错误.
故选A.
点评:本题考查弱电解质的电离,题目难度不大,本题注意醋酸为弱电解质,浓度不同,电离程度不同,浓度越大,电离程度越小的特征.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
当物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液中所含Cl-的个数比为1:1:1时,这三种溶液的体积比为( )
| A、2:3:6 |
| B、1:2:3 |
| C、3:2:1 |
| D、6:3:2 |
一定温度下,下列溶液的离子浓度关系式正确的是( )
| A、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol?L-1 |
| B、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C、pH=2的H2S溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HS-) |
| D、pH相同的①CH3COONa②NaHCO3两种溶液的c(Na+):①>② |
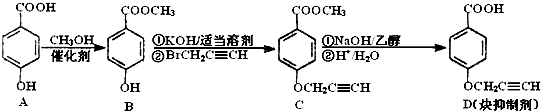
下列物质中互为同分异构体的是( )
| A、O2和O3 |
B、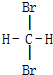 和 和 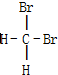 |
| C、CH3COOH和HCOOCH3 |
D、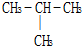 和 和 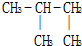 |
下列有关物质用途的说法中,不正确的是( )
| A、液氨可用做致冷剂,碱石灰可用于干燥氨气 |
| B、铁制器皿可用于盛放稀硫酸 |
| C、小苏打可用于治疗胃酸过多 |
| D、氯气可用于自来水消毒 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:对上述流程中的判断正确的是( )
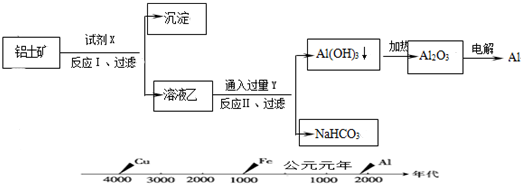

| A、试剂X为稀硫酸 |
| B、反应Ⅱ中生成Al(OH)3的反应为:CO2+2AlO2-+3H2O═2Al(OH)3↓+CO32- |
| C、人类对金属的使用历史与金属活动顺序和冶炼的难易程度有关 |
| D、Al2O3熔点很高,电解耗能大,可采用电解熔融AlCl3冶炼Al |
对于密闭容器中进行的反应:2NO2?N2O4,下列说法正确的是( )
| A、增大NO2的浓度,平衡常数增大 |
| B、增大N2O4的浓度,平衡常数增大 |
| C、增大NO2的浓度,正反应速率加快,逆反应速率减慢 |
| D、增大NO2的浓度,平衡常数不变 |