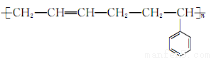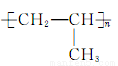题目内容
氧族元素(ⅥA族)的各种性质可归纳整理如下(部分):
元素 性质 | 8O | 16S | 34Se(硒) | 52Te(碲) |
单质沸 点(℃) | -183 | 444.6 | 685 | 1 390 |
主要 化合价 | -2 | -2,+4, +6 | -2,+4, +6 |
|
原子半 径(nm) | 0.074 | 0.102 | 0.116 | 0.143 |
单质与 H2反应 | 点燃易 化合 | 加热化合 | 加热 难化合 | 不能直 接化合 |
回答下列问题:
(1)氧原子的结构示意图为________,硫离子的结构示意图为________。
(2)碲的主要化合价可能有________。
(3)氧元素比硫元素的非金属性________(填“强”或“弱”)。请用化学方程式证明该结论:__________________________________________________________。
(4)H2O2被Cl2氧化生成O2,H2O2经常作脱氯剂,用于消除水中的Cl2,写出该反应的化学方程式:___________________。
(1)

(2)-2、+4、+6
(3)强 2Na2S+O2+2H2O===4NaOH+2S↓(合理即可)
(4)Cl2+H2O2===2HCl+O2
【解析】
试题分析:同主族元素性质相似,所以碲的主要化合价与S、Se可能相同。同主族元素,随原子序数的递增非金属性减弱,可用单质间的置换反应、氧化反应、氢化物的稳定性等进行证明。H2O2作脱氯剂时,被Cl2氧化生成O2,据此可写出对应的化学方程式。
考点:元素周期表、元素周期率。

下列四组溶液仅用所选的一种试剂(可加热)不能区别开的是( )
选项 | 所选的鉴别试剂 | 被鉴别的一组物质 |
A | 硫酸 | 碳酸钠溶液、硫化钠溶液、氯化钡溶液、食盐水 |
B | 烧碱溶液 | 硫酸铵溶液、硫酸铜溶液、氯化镁溶液、明矾溶液 |
C | FeCl3溶液 | 硝基苯、苯酚溶液、溴苯、石灰水、碳酸钠溶液 |
D | 水 | 电石、大理石、硫酸铜、硫酸镁 |
 的溶液:K+、Ba2+、NO3-、AlO-2
的溶液:K+、Ba2+、NO3-、AlO-2 
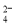

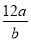 B.m g该氯原子的物质的量是
B.m g该氯原子的物质的量是 mol
mol
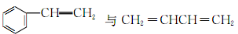 制高聚物
制高聚物