题目内容
| |||||||||||||||
答案:1.+1;2.CuI,0.5;3.2,5,2,1;
解析:
解析:
(1) |
反应中Hg是还原剂,化合价由0价升高到+2价,在反应产物Cu2HgI4中碘为-1价,由2x+2+(-1)×4=0,x=+1,即Cu元素显+1价. |
(2) |
由所给反应知由CuI→Cu化合价从+1降到0,所以CuI为氧化剂.由 |
(3) |
用化合价升降法配平: |

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸上颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI+Hg═Cu2HgI4+2Cu,下列说法正确的是( )
| A、CuI在反应中失去电子 | B、Cu2HgI4中Cu元素的化合价为+2 | C、CuI是氧化剂 | D、1mol CuI参与反应有1mol电子转移 |
液态金属汞常温下即可蒸发,其蒸气有剧毒,实验室为监测空气中汞蒸气的含量,通常悬挂有CuI的滤纸,根据滤纸是否变色或颜色发生变化的时间来判断空气中汞的含量,其反应为:4CuI+Hg═Cu2HgI4+2Cu(I的化合价反应前后均为-1价的).下列有关说法不正确的是( )
| A、上述反应的产物Cu2HgI4中,Hg的化合价为+2 | B、上述反应中氧化剂是CuI | C、上述反应中Cu元素仅有一半被还原 | D、上述反应中生成64g Cu时,转移的电子数为2NA |
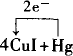
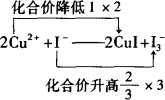 然后根据电荷守恒,观察配平I-的化学计量数.
然后根据电荷守恒,观察配平I-的化学计量数. Cl- OH- CO
Cl- OH- CO B.Fe2+ NO3- Cl- H+
B.Fe2+ NO3- Cl- H+
 Cu2++
Cu2++