题目内容
将一定质量的![]() 和
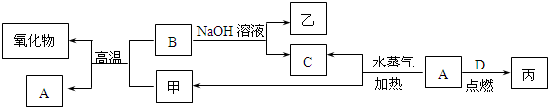
和![]() 混合物加热灼烧至恒重,将产生的气体通入足量的饱和石灰水中,充分反应后得到沉淀1.0 g.再将灼烧后的剩余固体物质与足量盐酸反应,生成气体2.2 g.计算原混合物中Na2CO3和NaHCO3的质量比.
混合物加热灼烧至恒重,将产生的气体通入足量的饱和石灰水中,充分反应后得到沉淀1.0 g.再将灼烧后的剩余固体物质与足量盐酸反应,生成气体2.2 g.计算原混合物中Na2CO3和NaHCO3的质量比.
答案:2.15∶1
解析:
解析:
根据CO2与石灰水的反应,生成CaCO3沉淀1.0克, 即 那么参加反应的 再根据灼烧后剩余的Na2CO3与盐酸充分反应后生成CO2 2.2克。 得到参加反应的 减去其中由 即原混合物中
|

练习册系列答案
相关题目
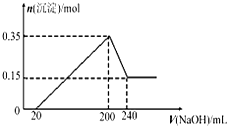 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )| A、Mg和Al的总质量为9g | B、生成的H2在标准状况下的体积为11.2L | C、NaOH溶液的物质的量浓度为5mol/L | D、硫酸的物质的量浓度为1mol/L |