题目内容
根据下列三个反应的化学方程式,下列关系式正确的是
①I2+SO2+2H2O=H2SO4+2HI ②2FeCl3+2HI=2FeCl2+2HCl+I2 ③2FeCl2+Cl2=2FeCl3.
- A.氧化性:Fe3+>Cl2>H2SO4>I2
- B.还原性:SO2>I->Fe2+>Cl-
- C.Fe与I2化合:2Fe+3I2=2FeI3
- D.FeI2溶液中通入一定量的Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B
分析:A、根据氧化剂的氧化性大于氧化产物的氧化性来分析;
B、根据还原剂的还原性大于还原产物的还原性来分析;
C、Fe3+与I-发生氧化还原反应;
D、根据氯气应优先氧化碘离子来分析.
解答:①I2+SO2+2H2O=H2SO4+2HI中氧化性I2>H2SO4,还原性SO2>I-,
②2FeCl3+2HI=2FeCl2+2HCl+I2中氧化性Fe3+>I2,还原性I->Fe2+,
③2FeCl2+Cl2=2FeCl3中氧化性Cl2>Fe3+,还原性Fe2+>Cl-,
A、氧化性大小为Cl2>Fe3+>I2>H2SO4,故A错误;
B、还原性大小为SO2>I->Fe2+>Cl-,故B正确;
C、因Fe3+与I-发生氧化还原反应,则Fe与I2化合发生Fe+I2=FeI2,故C错误;
D、氯气应优先氧化碘离子,氯气少量时发生2I-+Cl2=I2+Cl-,氯气过量时发生Fe2++2I-+2Cl2=Fe3++I2+4Cl-,故D错误;
故选B.
点评:本题考查氧化还原反应中氧化性、还原性的比较,并利用性质来分析发生的氧化还原反应,难度较大.
分析:A、根据氧化剂的氧化性大于氧化产物的氧化性来分析;
B、根据还原剂的还原性大于还原产物的还原性来分析;
C、Fe3+与I-发生氧化还原反应;
D、根据氯气应优先氧化碘离子来分析.
解答:①I2+SO2+2H2O=H2SO4+2HI中氧化性I2>H2SO4,还原性SO2>I-,
②2FeCl3+2HI=2FeCl2+2HCl+I2中氧化性Fe3+>I2,还原性I->Fe2+,
③2FeCl2+Cl2=2FeCl3中氧化性Cl2>Fe3+,还原性Fe2+>Cl-,
A、氧化性大小为Cl2>Fe3+>I2>H2SO4,故A错误;
B、还原性大小为SO2>I->Fe2+>Cl-,故B正确;
C、因Fe3+与I-发生氧化还原反应,则Fe与I2化合发生Fe+I2=FeI2,故C错误;
D、氯气应优先氧化碘离子,氯气少量时发生2I-+Cl2=I2+Cl-,氯气过量时发生Fe2++2I-+2Cl2=Fe3++I2+4Cl-,故D错误;
故选B.
点评:本题考查氧化还原反应中氧化性、还原性的比较,并利用性质来分析发生的氧化还原反应,难度较大.

练习册系列答案
相关题目
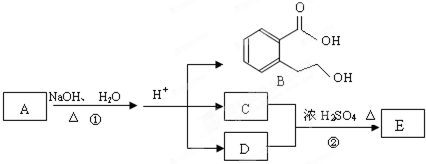

 任意1种
任意1种