题目内容
向氯化铁、氯化铜的混合液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A、溶液中一定含有Cu2+ |
| B、溶液中一定含有Fe2+ |
| C、加入KSCN溶液一定不变红色 |
| D、剩余固体中一定含有铜 |
考点:铁的化学性质
专题:
分析:根据FeCl3、CuCl2的氧化性强弱判断反应先后顺序,从而确定固体的成分、溶液的成分.
解答:
解:分阶段分析
①、当固体为铁、铜时,溶液中的Fe3+、Cu2+全部参加反应生成Fe2+和Cu,反应的反应方程式为:2FeCl3+Fe=3FeCl2
CuCl2+Fe=Cu+FeCl2
所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+;
②当固体为铜时,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,
所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
A、通过以上分析知,溶液中可能含有Cu2+,故A错误;
B、通过以上分析知,溶液中一定含有Fe2+,故B正确;
C、溶液中一定不含Fe3+,所以加入KSCN溶液不变红色,故C正确;
D、通过以上分析知,剩余固体中一定含Cu,故D正确.
故选A.
①、当固体为铁、铜时,溶液中的Fe3+、Cu2+全部参加反应生成Fe2+和Cu,反应的反应方程式为:2FeCl3+Fe=3FeCl2
CuCl2+Fe=Cu+FeCl2
所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+;
②当固体为铜时,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,
所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
A、通过以上分析知,溶液中可能含有Cu2+,故A错误;
B、通过以上分析知,溶液中一定含有Fe2+,故B正确;
C、溶液中一定不含Fe3+,所以加入KSCN溶液不变红色,故C正确;
D、通过以上分析知,剩余固体中一定含Cu,故D正确.
故选A.
点评:本题考查了Fe3+、Cu2+的氧化能力大小的比较,能正确判断固体的成分是解本题的关键,根据固体的成分了解反应的先后顺序,从而确定溶液的成分.

练习册系列答案
相关题目
化合物A、B、C都只含有两种元素,且A、B均含X元素,已知一定条件下可发生反应:A+B→C+X,X是一种单质,由此可知( )
| A、X一定是金属元素 |
| B、X一定是非金属元素 |
| C、X可能是金属元素,也可能是非金属元素 |
| D、A、B中X的化合价均高于0 |
关于下列实验的叙述合理的是( )
| A、某氢化物的溶液能使石蕊试液变蓝,该氢化物一定是氨气 |
| B、将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 |
| C、配制硫酸亚铁溶液时应将硫酸亚铁固体溶于浓硫酸中,再稀释至所需浓度,以防止水解 |
| D、配制银氨溶液应将稀氨水逐滴滴入到硝酸银溶液中至产生的沉淀刚好溶解 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲
乙
丙.下列有关物质的推断不正确的是( )
| 丁 |
| 丁 |
| 甲 |
| A、若甲为Cl2,则丁可能是铁 |
| B、若甲为NH3,则丁可能是氧气 |
| C、若甲为AlCl3溶液,则丁可能是氨水 |
| D、若甲为NaOH,则丁可能是SO2 |
下列各组混合物能用分液漏斗直接分离的是( )
| A、苯和四氯化碳 | B、汽油和水 |
| C、碘和水 | D、水和乙醇 |
将2×10-5mol/LKCl 与2×10-5mol/LAgNO3溶液等体积混合,下列说法正确的是(已知AgCl的Ksp=1.8×10-10)( )
| A、有AgCl沉淀析出 |
| B、无AgCl沉淀 |
| C、无法确定 |
| D、有沉淀但不是AgCl |
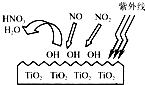 还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.
还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.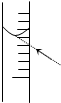 用18.4mol?L-1的浓H2SO4配制100mL浓度为1mol?L-1 H2SO4,其操作可分为以下几步:
用18.4mol?L-1的浓H2SO4配制100mL浓度为1mol?L-1 H2SO4,其操作可分为以下几步: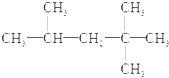 某有机物化合物A的结构简式如图完成下列问题:
某有机物化合物A的结构简式如图完成下列问题: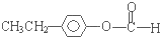 、
、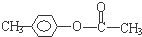 ,写出另外两种的结构简式:
,写出另外两种的结构简式: