题目内容
10.在一定温度下,向a L密闭容器中加入1mol H2(g)和1mol Br2(g),发生如下反应:H2(g)+Br2(g)?2HBr(g),此反应达到平衡的标志是( )| A. | 容器内颜色不随时间变化 | |
| B. | 容器内H2、Br2、HBr的浓度之比为1:1:2 | |
| C. | 容器内压强不随时间变化 | |
| D. | 单位时间内消耗n mol H2,同时消耗2n mol HBr |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.该反应中只有溴是有色物质,当容器内颜色不随时间变化时,说明溴的物质的量不变,则该反应达到平衡状态,故A正确;
B.容器内H2、Br2、HBr的浓度之比为1:1:2时,该反应不一定达到平衡状态,与反应初始浓度及转化率有关,故B错误;
C.该反应前后气体计量数之和不变,则无论反应是否达到平衡状态,容器内压强始终不变,所以不能根据压强判断平衡状态,故C错误;
D.单位时间内消耗n mol H2,同时生成2nmolHBr,因为同时消耗2n mol HBr,则HBr正逆反应速率相等,所以该反应达到平衡状态,故D正确;
故选AD.
点评 本题考查化学平衡状态判断,为高频考点,只有反应前后改变的物理量才能作为平衡状态判断依据,注意该反应前后气体计量数之和不变,不能根据压强判断平衡状态,为易错点.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案
相关题目
20.只用一种试剂来鉴别碳酸钠、亚硫酸钠、硫酸钠,这种试剂可以是( )
| A. | BaCl2 | B. | 溴水 | C. | 稀盐酸 | D. | 品红溶液 |
18.下列标有横线的物质在给定条件下能完全溶解的是( )
| A. | 常温下,1mol Zn与含1mol浓硫酸反应 | |
| B. | 加热条件下,1mol Cu与含2mol浓硫酸反应 | |
| C. | 常温下,1mol Cu与含4mol浓硝酸反应 | |
| D. | 加热条件下,1mol MnO2与含4mol浓盐酸反应 |
5.既含有极性共价键又含有非极性共价键的物质是( )
| A. | 甲烷 | B. | 乙烷 | C. | 水 | D. | 氧气. |
2.如图是某含C、H、O、N四种元素的有机分子的球棍模型.下列有关该有机物的说法错误的是( )
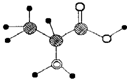

| A. | 其结构简式为:CH3CH(NH2)COOH | |
| B. | 该有机物含有两种官能团 | |
| C. | 该有机物的核磁共振氢谱显示7个吸收峰 | |
| D. | 该有机物能跟NaHCO3溶液反应产生CO2气体 |
20.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L水含有NA个H2O分子 | |
| B. | 1mol.L-1 Na2CO3溶液中含有Na+数目为2NA | |
| C. | 常温常压下,22.4LO2中含有2NA个氧原子 | |
| D. | 16g O2 和O3的混合气体中含氧原子数目为NA |

 .
.