题目内容
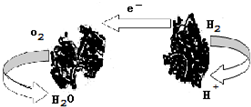 如图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气体可以混合从而省去了昂贵的燃料隔离膜.下列对其工作原理叙述正确的是( )
如图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气体可以混合从而省去了昂贵的燃料隔离膜.下列对其工作原理叙述正确的是( )分析:由电池示意图可知,H2→H+,是H2被氧化的过程,通入H2的一极为原电池的负极,电极反应式为H2-2e-=2H+,有氢离子生成,所以电解质溶液为酸性溶液,O2→H2O,是O2被还原的过程,通入O2的一极为原电池的正极,电极反应式为O2+4e-+4H+=2H2O,其电池反应式为2H2+O2=2H2O,以此解答该题.
解答:解:A.该燃料电池的电池反应式为2H2+O2=2H2O,电解质溶液中氢离子的物质的量不变,但溶液的体积增大,所以氢离子浓度逐渐减小,故A错误;
B.该电池包括两个涂覆着酶的电极,高温下会使酶变性,不能在高温下使用,故B错误;
C.通入H2的一极为原电池的负极,发生:H2-2e-=2H+,故C正确;
D.通入O2的一极为原电池的正极,发生:O2+4e-+4H+=2H2O,故D错误.
故选C.
B.该电池包括两个涂覆着酶的电极,高温下会使酶变性,不能在高温下使用,故B错误;
C.通入H2的一极为原电池的负极,发生:H2-2e-=2H+,故C正确;
D.通入O2的一极为原电池的正极,发生:O2+4e-+4H+=2H2O,故D错误.
故选C.
点评:本题考查化学电源新型电池,根据图片中电子流动方向及反应物和生成物来确定正负极,注意把握题给信息为解答该题的关键,能根据生成物判断电极反应并书写电极方程式,难度中等.

练习册系列答案
相关题目
 三层复合石头纸是一种新型纸张,其结构如图所示:上下两层为聚乙烯,中间层为碳酸钙.下列关于它的叙述错误的是( )
三层复合石头纸是一种新型纸张,其结构如图所示:上下两层为聚乙烯,中间层为碳酸钙.下列关于它的叙述错误的是( )| A、易生物降解 | B、可替代木浆纸以减少树木砍伐 | C、与普通纸相比难以燃烧 | D、具有防水防油的特性 |












 (1)SO2的排放是造成酸雨的主要因素.某地区酸雨pH随时间的变化如右图所示.请用化学方程式表示该地区酸雨pH随时间增加而减小的原因
(1)SO2的排放是造成酸雨的主要因素.某地区酸雨pH随时间的变化如右图所示.请用化学方程式表示该地区酸雨pH随时间增加而减小的原因