题目内容
18.在一接近中性的含Na+的澄清溶液中,可能还含NH4+;Fe2+;I-;Br-;CO32-;SO32-六种离子中的几种.①在原溶液中,滴加足量氯水后,有气泡产生;溶液呈橙黄色;②向呈橙黄色溶液中加入BaCl2溶液时无沉淀生成;③橙黄色溶液不能使淀粉变蓝色.根据上述实验事实推断,该溶液中肯定不存在的离子是( )| A. | NH4+、Br-、CO32- | B. | Fe2+、I-、SO32- | C. | NH4+、Br-;、SO32- | D. | Fe2+、I-、CO32- |
分析 ①在原溶液中滴加足量的饱和氯水后,有气泡生成,说明溶液中含有CO32-,则一定不存在Fe2+,溶液呈橙黄色,说明可能生成I2或Br2;
②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成,说明不含SO32-;
③橙黄色溶液不能使淀粉溶液变蓝色,说明不含I-.
解答 解:根据①可知溶液中含有CO32-,则一定不存在Fe2+,溶液呈橙黄色,说明可能生成I2或Br2;
根据②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成,说明不含SO32-;
根据③橙黄色溶液不能使淀粉溶液变蓝色可知溶液中不含I-;
所以溶液中一定存在Br-、CO32-,一定不存在Fe2+、I-、SO32-,
故选B.
点评 本题考查离子的检验,题目难度不大,明确常见离子的性质为解答关键,注意通过反应的现象结合离子的性质进行推断,要排除实验操作的干扰.

练习册系列答案
相关题目
4.下列离子方程式书写正确的是( )
| A. | 铁与稀硫酸反应 Fe+2H+═Fe3++H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 碳酸钡与盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| D. | 氢氧化钠溶液与硫酸铜溶液反应 2OH-+Cu2+═Cu(OH)2↓ |
5.下列对实验现象的解释与结论正确的是( )
| A. | 向铜和稀硫酸的混合物中加入某无色溶液,溶液逐渐变成蓝色,铜逐渐溶解,则该无色溶液一定是硝酸 | |
| B. | 用蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口,有大量白烟,说明该无机酸一定为盐酸 | |
| C. | SO2气体通入Ba(NO3)2溶液中,溶液出现浑浊现象,说明有BaSO3沉淀生成 | |
| D. | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色,说明Fe3+的氧化性大于I2 |
6.下列实验原理或操作,正确的是( )
| A. | 用广泛pH试纸测得 0.1mol/L NH4Cl溶液的pH=5.2 | |
| B. | 酸碱中和滴定时锥形瓶用蒸馏水洗涤后,再用待测液润洗后装液进行滴定 | |
| C. | 将碘水倒入分液漏斗,加入适量苯振荡后静置,从分液漏斗放出碘的苯溶液 | |
| D. | 在溴化钠中加入少量的乙醇,再加入2倍于乙醇的1﹕1的硫酸制取溴乙烷 |
10.下列物质在常温下发生水解时,对应的水解方程式正确的是( )
| A. | Na2CO3:CO32-+H2O?2OH-+CO2↑ | B. | NH4NO3:NH4++H2O?NH3•H2O+H+ | ||
| C. | CuSO4:Cu2++2H2O?Cu(OH)2↓+2H+ | D. | KF:F-+H2O═HF+OH- |
7.“低碳生活”是指减少能源消耗、节约资源,从而减少二氧化碳排放的生活方式.下列不符合“低碳生活”的做法是( )
| A. | 自驾车代替骑自行车出行 | B. | 环保袋代替一次性塑料袋 | ||
| C. | 太阳能热水器代替燃气热水器 | D. | 节能灯代替白炽灯 |
8.下列物质分类正确的是( )
| A. | Na2O2、Fe3O4、CuO均为碱性氧化物 | B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | ||
| C. | 烧碱、冰醋酸、四氯化碳均为电解质 | D. | 盐酸、水玻璃、氨水均为混合物 |
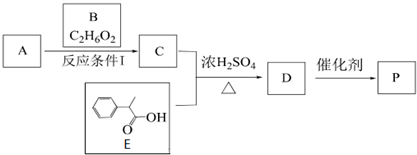
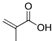 ,E的化学式为C9H10O2
,E的化学式为C9H10O2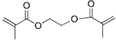
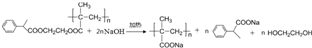 .
.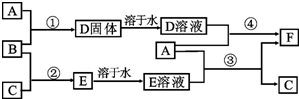 A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示.
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示.