题目内容
【题目】铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示.已知活性炭对重金属离子具有一定的吸附作用.
(1)当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+ , 其原因是 .
(2)当铁炭混合物中铁的质量分数相同时,Cu2+的去除率比Pb2+的高,其主要原因是 .
(3)纳米铁粉可用于处理地下水中的污染物.
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4﹣(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4﹣ , 其离子方程式为 .
②纳米铁粉与水中NO3﹣反应的离子方程式为 4Fe+NO3﹣+10H+═4Fe2++NH4++3H2O 研究发现,若pH偏低将会导致NO3﹣的去除率下降,其原因是 . 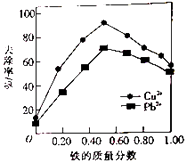
【答案】
(1)活性炭对Cu2+和Pb2+具有吸附作用
(2)Cu2+的氧化性比Pb2+的强
(3)2Fe2++BH4﹣+4OH﹣=2Fe+2H2↑+B(OH)4﹣;纳米铁粉与H+反应生成H2
【解析】解:(1)当铁炭混合物中铁的质量分数为0时,则只有碳粉,可去除水中少量的Cu2+和Pb2+ , 原因是碳粉具有吸附性,也可起到净水的作用,所以答案是:活性炭对Cu2+和Pb2+具有吸附作用;(2)Cu2+的氧化性比Pb2+的强,易与铁发生氧化反应,则当铁炭混合物中铁的质量分数相同时,Cu2+的去除率比Pb2+的高,
所以答案是:Cu2+的氧化性比Pb2+的强;(3)①向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4﹣(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4﹣ , 反应中只有Fe、H元素化合价发生变化,发生氧化还原反应,离子方程式为2Fe2++BH4﹣+4OH﹣=2Fe+2H2↑+B(OH)4﹣ ,
所以答案是:2Fe2++BH4﹣+4OH﹣=2Fe+2H2↑+B(OH)4﹣;
②pH偏低,氢离子浓度偏大,则铁可与氢离子反应生成氢气,可导致NO3﹣的去除率下降,所以答案是:纳米铁粉与H+反应生成H2 .