题目内容
A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径A>B; ②离子半径A>B; ③A的正价与B的负价绝对值一定相等;④电负性A<B; ⑤第一电离能A>B.
其中正确的组合是( )
①原子半径A>B; ②离子半径A>B; ③A的正价与B的负价绝对值一定相等;④电负性A<B; ⑤第一电离能A>B.
其中正确的组合是( )
| A、①④ | B、①②③ |
| C、①④⑤ | D、②③⑤ |
考点:原子结构与元素周期律的关系
专题:
分析:A元素的阳离子与B元素的阴离子具有相同的电子层结构,则A元素位于B元素下一周期,A属于金属元素、B元素属于非金属元素,
①电子层数越多,其原子半径越大;
②电子层结构相同的离子,离子半径随着原子序数增大而减小;
③A的正价与B的负价绝对值不一定相等;
④同一周期,元素的电负性随着原子序数增大而增大,同一主族元素,元素的电负性随着原子序数增大而减小;
⑤同一周期元素,元素的第一电离能随着原子序数增大而呈增大趋势,同一主族,元素的第一电离能随着原子序数增大而减小.
①电子层数越多,其原子半径越大;
②电子层结构相同的离子,离子半径随着原子序数增大而减小;
③A的正价与B的负价绝对值不一定相等;
④同一周期,元素的电负性随着原子序数增大而增大,同一主族元素,元素的电负性随着原子序数增大而减小;
⑤同一周期元素,元素的第一电离能随着原子序数增大而呈增大趋势,同一主族,元素的第一电离能随着原子序数增大而减小.
解答:
解:A元素的阳离子与B元素的阴离子具有相同的电子层结构,则A元素位于B元素下一周期,A属于金属元素、B元素属于非金属元素,
①电子层数越多,其原子半径越大,A的电子层数大于B,所以原子半径A>B,故正确;
②电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径B>A,故错误;
③A的正价与B的负价绝对值不一定相等,如Na+和O 2-,故错误;
④同一周期,元素的电负性随着原子序数增大而增大,同一主族元素,元素的电负性随着原子序数增大而减小,元素的非金属性越强,其电负性越强,所以电负性A<B,故正确;
⑤同一周期元素,元素的第一电离能随着原子序数增大而呈增大趋势,同一主族,元素的第一电离能随着原子序数增大而减小,所以第一电离能A<B,故错误;
故选A.
①电子层数越多,其原子半径越大,A的电子层数大于B,所以原子半径A>B,故正确;
②电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径B>A,故错误;
③A的正价与B的负价绝对值不一定相等,如Na+和O 2-,故错误;
④同一周期,元素的电负性随着原子序数增大而增大,同一主族元素,元素的电负性随着原子序数增大而减小,元素的非金属性越强,其电负性越强,所以电负性A<B,故正确;
⑤同一周期元素,元素的第一电离能随着原子序数增大而呈增大趋势,同一主族,元素的第一电离能随着原子序数增大而减小,所以第一电离能A<B,故错误;
故选A.
点评:本题考查原子结构和元素周期律的关系,涉及电负性、第一电离能、原子半径、离子半径等知识点,熟练掌握元素周期律并灵活运用,注意规律中的异常现象,题目难度不大.

练习册系列答案
相关题目
下列做法不利于食品安全的是( )
| A、在食盐中添加适量的碘酸钾 |
| B、用甲醛浸泡食品,使其不易变质 |
| C、在食品加工中科学地使用食品添加剂 |
| D、研发高效低毒的农药,降低蔬菜的农药残留量 |
关于CH4和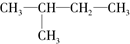 的叙述正确的是( )
的叙述正确的是( )
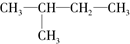 的叙述正确的是( )
的叙述正确的是( )| A、均能用CnH2n+2组成来表示 |
| B、与所有烷烃互为同素异形体 |
| C、因为它们结构相似,所以它们的化学性质相似,但物理性质不相同 |
| D、通常状况下它们都是气态烷烃 |
下列说法不正确的是( )
| A、“白色污染”主要是由合成材料的废弃物,特别是一些塑料制品废弃物造成的 |
| B、“白色污染”只能影响环境卫生,没有其他危害 |
| C、治理“白色污染”主要应从减少使用、加强回收和再利用开始 |
| D、使用可降解塑料是治理“白色污染”的理想方法 |
下列实验现象的描述正确的是( )
| A、氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾 |
| B、氧化铁溶于水生成红褐色沉淀 |
| C、铜在氯气中燃烧,产生棕黄色烟 |
| D、钠在空气中燃烧,发出黄色的火焰,生成白色固体 |
下表为4种常见溶液中溶质的质量分数和物质的量浓度:这4种溶液中密度最小的是( )
| 溶 质 | HCl | NaOH | CH3COOH | HNO3 |
| 溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
| 物质的量浓度/mol L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
| A、HCl |
| B、NaOH |
| C、CH3COOH |
| D、NO3 |
下列关于 0.2mol/L 硝酸钾溶液的叙述中,正确的是( )
| A、1L 该溶液中含硝酸钾 202g |
| B、100mL 该溶液中含硝酸钾0.02mol |
| C、从 1L该溶液中取出500 mL 后,剩余溶液的浓度为0.1mol/L |
| D、1L水中溶解0.2mol硝酸钾,即可配得 0.2mol/L硝酸钾溶液 |
下列关于碳、硅及其化合物的叙述中,正确的是( )
| A、碳、硅都是较活泼的非金属,它们只能以化合态存在于自然界中 |
| B、等质量的Na2CO3、NaHCO3分别与足量盐酸反应,前者产生的CO2多 |
| C、一定条件下CO2、SiO2都能与NaOH、Na2CO3(或CaCO3)发生反应 |
| D、热稳定性:CH4<SiH4;酸性H2CO3>H2SiO3(H4SiO4) |