题目内容
4.下列各组的两种物质在溶液中反应,可用同一离子方程式表示的是( )| A. | Cu(OH)2和HCl; Cu(OH)2和CH3COOH | |
| B. | Ba(OH)2和MgSO4; BaCl2和(NH4)2SO4 | |
| C. | Na2CO3和H2SO4; K2CO3和NaHSO4 | |
| D. | CaCO3和HCl; Na2CO3和HCl |
分析 A.CH3COOH为弱酸,应写成化学式,HCl为强电解质,写成离子;
B.氢氧化钡与硫酸镁反应除了生成硫酸钡沉淀,还生成了氢氧化镁沉淀;
C.两个反应实质都是碳酸根离子与氢离子反应生成二氧化碳和水;
D.碳酸钙为难溶物,离子方程式中不能拆开.
解答 解:A.Cu(OH)2和HCl反应的离子方程式为:Cu(OH)2+2H+=Cu2++2H2O,Cu(OH)2和CH3COOH反应的离子方程式为:Cu(OH)2+2CH3COOH=Cu2++2H2O+2CH3COO-,二者不同,故A错误;
B.Ba(OH)2和MgSO4的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,BaCl2和(NH4)2SO4的离子方程式为:SO42-+Ba2+=BaSO4↓,二者不同,故B错误;
C.Na2CO3和H2SO4、K2CO3和NaHSO4的离子方程式都是:2H++CO32-=H2O+CO2↑,故C正确;
D.CaCO3和HCl的离子方程式为:2H++CaCO3=Ca2++H2O+CO2↑,Na2CO3和HCl的离子方程式为:2H++CO32-=H2O+CO2↑,两个离子方程式不同,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高考经典题型,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
14.25℃时,将a g硫酸铜晶体(CuSO4•5H2O)溶于b g水中,恰好形成V mL饱和溶液.下列关系不正确的是( )
| A. | 该饱和溶液硫酸铜物质的量浓度为c=$\frac{4a}{v}$ mol•L-1 | |
| B. | 该饱和溶液中硫酸铜的质量分数为w=$\frac{16a}{a+b}$% | |
| C. | 25℃硫酸铜的溶解度为 S=$\frac{1600a}{9a+25b}$g | |
| D. | 该饱和硫酸铜溶液的密度为ρ=$\frac{a+b}{v}$g•L-1 |
15.某广告称某种牌号的八宝粥(含桂圆、红豆、糯米等)不加糖,比加糖还甜,最适合糖尿病人食用.你认为下列关于糖尿病人能否食用此八宝粥的判断正确的是( )
| A. | 这个广告有误导喜爱甜食的消费者的嫌疑,不加糖不等于没有糖 | |
| B. | 不加糖不等于没有糖,糖尿病人食用需慎重 | |
| C. | 不能只听从厂商或广告商的宣传,应咨询医生 | |
| D. | 糖尿病人应少吃含糖的食品.该八宝粥未加糖,可以放心食用 |
12.下列反应的离子方程式书写正确的是( )
| A. | 氯化铁溶液与铜反应:Fe3++Cu═Fe2++Cu2+ | |
| B. | 硅酸钠与稀硫酸反应:Na2SiO3+2H+═2Na++H2SiO3↓ | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化镁与稀盐酸反应:Mg(OH)2+2H+═Mg2++2H2O |
19. A~E是核电荷数均小于20的元素,其结构或性质信息如下表
A~E是核电荷数均小于20的元素,其结构或性质信息如下表
请根据表中的信息回答下列问题:
(1)D离子的结构示意图: ,B原子的电子式:
,B原子的电子式: ,E离子的电子式:
,E离子的电子式: .
.
(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种:CH4,H2O.
(3)A元素与E元素组成的化合物的电离方程式:HCl=H++Cl-.
(4)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是钾元素的相对原子质量;写出钾离子的电子式:K+.
 A~E是核电荷数均小于20的元素,其结构或性质信息如下表
A~E是核电荷数均小于20的元素,其结构或性质信息如下表| 元素 | A | B | C | D | E |
| 性质或结构信息 | 其原子核内只有1个质子 | 其单质在空气中体积含量最多 | 其原子M层有3个电子 | 食盐中的金属元素 | 单质在常温、常压下是黄绿色的气体 |
(1)D离子的结构示意图:
 ,B原子的电子式:
,B原子的电子式: ,E离子的电子式:
,E离子的电子式: .
.(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种:CH4,H2O.
(3)A元素与E元素组成的化合物的电离方程式:HCl=H++Cl-.
(4)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是钾元素的相对原子质量;写出钾离子的电子式:K+.
9.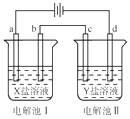 如图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
如图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
 如图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
如图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )| 选项 | X | Y |
| A | MgSO4 | CuSO4 |
| B | CuSO4 | AgNO3 |
| C | FeSO4 | Al2(SO4)3 |
| D | AgNO3 | Pb(NO3)2 |
| A. | A | B. | B | C. | C | D. | D |
16.下列溶液中的Cl-浓度与50mL1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150mL1mol•L-1NaCl溶液 | B. | 75mL1mol•L-1CaCl2溶液 | ||
| C. | 150mL1mol•L-1KCl溶液 | D. | 75mL1mol•L-1AlCl3溶液 |
7.水泥和陶瓷工业的共同原料是下列物质中的( )
| A. | 黏土 | B. | 石灰石 | C. | 长石 | D. | 石英 |
8.工业上常使用电解精炼法将粗铜提纯.在电解精炼铜时( )
| A. | 粗铜接电源负极 | |
| B. | 纯铜作阳极 | |
| C. | 杂质都将以单质形式沉积到池底 | |
| D. | 纯铜片增重2.56 g,电路中通过电子为0.08 mol |