题目内容
3.下列离子方程式正确的是( )| A. | 向FeI2溶液中通入等物质的量的Cl2:2I-+Cl2═2Cl-+I2 | |
| B. | 用过量氨水吸收烟道气中的SO2:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 向NaHSO4溶液中加入Ba(OH)2至中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| D. | 向AgCl饱和溶液中滴加Na2S溶液:2AgCl+S2-═Ag2S+2Cl- |
分析 A.碘离子的还原性强于二价铁离子,氯气先氧化碘离子;
B.二氧化硫少量,反应生成亚硫铵;
C.向NaHSO4溶液中加入Ba(OH)2至中性,二者物质的量之比2:1;
D.向AgCl饱和溶液中滴加Na2S溶液,反应生成硫化银沉淀和氯离子.
解答 解:A.向FeI2溶液中通入等物质的量的Cl2:,氯气少量只氧化碘离子,离子方程式:2I-+Cl2═2Cl-+I2,故A正确;
B.用过量氨水吸收烟道气中的SO2,离子方程式:SO2+2NH3•H2O═SO32-+2NH4+,故B错误;
C.向NaHSO4溶液中加入Ba(OH)2至中性,二者物质的量之比2:1,离子方程式:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故C错误;
D.向AgCl饱和溶液中滴加Na2S溶液,离子方程式:2AgCl(s)+S2-(aq)═Ag2S(s)+2Cl-(aq),故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,选项BC为易错选项.

练习册系列答案
相关题目
13.化学在生产和生活中有重要的应用,下列说法不正确的是( )
| A. | 可溶性铁盐、铝盐均可用于水的净化 | |
| B. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 | |
| C. | 电解NaCl溶液可制得金属钠 | |
| D. | 在海轮外壳上镶嵌上锌块,可减缓船体的腐蚀速率 |
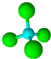
14. 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A. | 1molAl2H6中约含有4.8×1024个σ键 | |
| B. | 60gAl2H6中含铝原子约为1.2×1023个 | |
| C. | Al2H6可以燃烧,产物为氧化铝和水 | |
| D. | Al2H6在固态时所形成的晶体是离子晶体 |
18.100g样品所消耗的溴的毫克数称为溴指数.溴指数越高,则说明样品中不饱和烃含量越高.我国石油工业一般利用恒定电流库仑分析法测定汽油的溴指数,利用电解产生的溴与不饱和烃反应,支持电解质为LiBr,溶剂仅含5%的水,其余为甲醇,苯与醋酸.下列有关说法正确的是( )
| A. | 在溶剂中提高苯的比例,能提高溶液的导电性 | |
| B. | 电解时阳极的电极反应式为2Br--2e-=Br2 | |
| C. | 电解时可用铁作阳极材料 | |
| D. | 汽油样品应加在阴极区 |
6.下列晶体属于分子晶体的是( )
| A. | 石英 | B. | C60 | C. | NaCl | D. | 金属K |
4.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4L CCl4含有的分子数为NA | |
| B. | 常温常压下,17g NH3所含的原子数目为4NA | |
| C. | 铝与足量盐酸反应,生成2.24L H2时,转移的电子数为0.2NA | |
| D. | 0.1mol/L Na2CO3溶液中含有的Na+数目为0.2NA |
 H++H2PO4-、H2PO4-
H++H2PO4-、H2PO4- 
 .
.
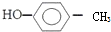
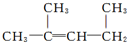 的名称:1,3-二甲基-2丁烯( )
的名称:1,3-二甲基-2丁烯( )