题目内容
工业上制纯碱是根据![]() 溶解度比NaCl、
溶解度比NaCl、![]() 、
、![]() 、
、![]() 都小的性质,在适宜温度下运用:
都小的性质,在适宜温度下运用:![]() +
+![]() +
+![]() +NaCl→
+NaCl→![]() +
+![]() 等反应原理制取的.欲在实验室通过上述过程和其它的必要反应制取纯碱,可用下列图示中的①②③④几个步骤,其中A、B分别代表
等反应原理制取的.欲在实验室通过上述过程和其它的必要反应制取纯碱,可用下列图示中的①②③④几个步骤,其中A、B分别代表![]() 和
和![]() 之一.
之一.
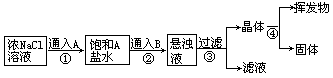
(1)操作③所得到的晶体是下列的________;
[ ]
A.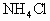
B.
C.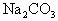
D.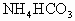
(2)对于上述过程,下面叙述错误的是________.
[ ]
A.气体A是![]() ,气体B是
,气体B是![]()
B.气体A是![]() ,气体B是
,气体B是![]()
C.步骤④是加热
D.①②两步操作的顺序与两种气体溶解度有重要的关系,不能颠倒
答案:B;A
解析:
解析:
|
解析:
实验过程④是将 (1)B;(2)A |

练习册系列答案
相关题目

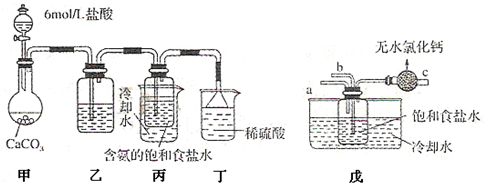

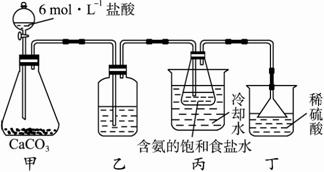
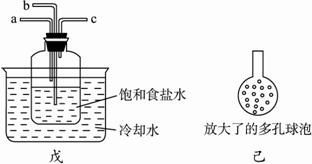
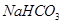 和
和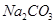 的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。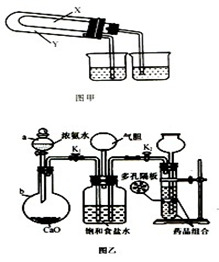
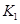 、
、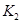 的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。 和
和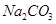 的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。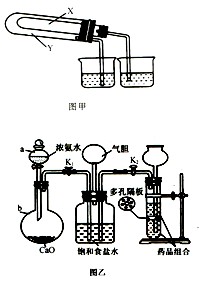
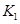 、
、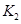 的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。