题目内容
碳酸钠俗称纯碱,是一种常用化学品。工业上制取碳酸钠的方法是:将二氧化碳和氨气通入饱和食盐水中,控制一定温度,制得碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠。有关反应的化学方程式为:?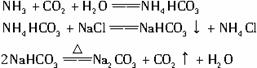
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________ (填标号)。
A.碳酸氢钠难溶于水?
B.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出?
C.碳酸氢钠受热易分解?
(2)某探究活动小组根据工业制取碳酸钠的原理,进行碳酸氢钠的制备实验, 同学们按各自设计的方案实验。?
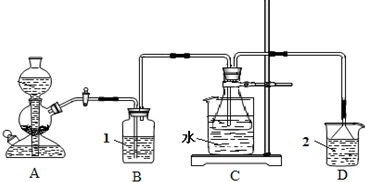
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。?

i.乙装置中的试剂是_______________(填标号)。?
A.烧碱溶液?
B.澄清石灰水?
C.浓氨水?
D.蒸馏水?
ii.丁装置的作用是_________________________。?
iii.实验结束后,分离出NaHCO3晶体的操作是_________________(填名称)。
②另一位同学用下图中戊装置(其他装置未画出)进行实验。
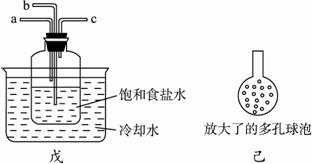
i.实验时,须先从a管通入_________气体,再从b管通入____________气体。?
ii.有同学建议在b管下端连接上图中己装置,理由是__________________________。?
(3)请你再写出一种实验室制取少量碳酸氢钠的方法。____________________________。
(1)B?
(2)①i.D?
ii.吸收NH3,防止出现倒吸?
iii.过滤?
②i.NH3 CO2?
ii.增大气体与溶液接解面积,提高CO2吸收率?
(3)用碳酸氢铵与适量饱和食盐水反应?
(注:或往烧碱溶液中通入过量 CO2;往饱和?Na2CO3?溶液中通入过量CO2等其他合理方法均可)
解析:
NaHCO3溶解度较小,故饱和NH4HCO3与食盐水反应析出NaHCO3晶体。?
(2)①乙应为除杂装置除去CO2中混有的HCl,应用蒸馏水,最好为饱和NaHCO3溶液。丁装置为一倒扣漏斗,目的防倒吸。而极易溶于水的只有NH3故防止NH3溶于水倒吸。NaHCO3晶体结晶析出,故应为过滤。?
②由侯氏制碱法推知必先通入NH3,后通入CO2,由于CO2能溶于水,溶解度较小,故已装置应为增大接触面积充分反应而设计的。?
(3)饱和溶液①NH4HCO3+NaCl══NaHCO3↓+NH4Cl?
②NaOH溶液中通入过量CO2。?
③Na2CO3溶液中通入过量CO2等。

 阅读快车系列答案
阅读快车系列答案| A、热的纯碱溶液常用于去除物品表面的油污 | B、相同温度下,纯碱的溶解度比小苏打的溶解度大 | C、物质的量浓度相同时,Na2CO3溶液的pH比NaHCO3溶液的大 | D、在医疗上,纯碱是治疗胃酸过多的一种药剂 |
| A、Na2CO3的稳定性介于Na2CO3?10H2O和NaHCO3之间 | B、“侯氏制碱法”制得的碱是指NaHCO3 | C、可用盐酸鉴别Na2CO3 和NaHCO3固体 | D、纯碱有时可代替烧碱使用,比如溶解石英、促进乙酸乙酯的水解等 |