题目内容
常温下,下列叙述错误的是
A.向0.1mol·L-1的醋酸溶液中加水或通入HCl气体都能使 值增大
值增大
B.0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合后溶液显酸性,则有

C.pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液
D.0.1mol·L-1某一元酸HA溶液中 ,则该溶液中由水电离出的
,则该溶液中由水电离出的 mol·L-1
mol·L-1
D
【解析】
试题分析:电离平衡常数不变,加水 减小,故
减小,故 增大;加盐酸,醋酸电离平衡逆向移动,
增大;加盐酸,醋酸电离平衡逆向移动, 减小,故
减小,故 增大,故A正确;0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合,得到等浓度醋酸、醋酸钠、氯化钠的混合溶液,溶液存在
增大,故A正确;0.1mol·L-1的醋酸钠溶液20mL与0.1mol·L-1盐酸10mL混合,得到等浓度醋酸、醋酸钠、氯化钠的混合溶液,溶液存在
 H++
H++ ,
, +H2O
+H2O OH—+
OH—+ ,溶液呈酸性,说明水解小于电离,c(
,溶液呈酸性,说明水解小于电离,c( ) >c(
) >c( ),c(
),c( )>c(H+),故B错误;常温下pH=4的醋酸与pH=10的氢氧化钠恰好完全反应生成醋酸钠,水解呈碱性,故C错误;常温下Kw=1×10-14 mol2/L2,
)>c(H+),故B错误;常温下pH=4的醋酸与pH=10的氢氧化钠恰好完全反应生成醋酸钠,水解呈碱性,故C错误;常温下Kw=1×10-14 mol2/L2, ,所以由水电离出的
,所以由水电离出的 mol·L-1,故D正确。
mol·L-1,故D正确。
考点:本题考查水溶液。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目


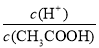 的比值将__________(填“增大”、“减小”或“无法确定”)。
的比值将__________(填“增大”、“减小”或“无法确定”)。 3C+5D反应中,表示该反应速率最快的是
3C+5D反应中,表示该反应速率最快的是