题目内容
1.下列实验操作或说法错误的是( )| A. | 蒸发时,蒸发皿中固体不能蒸干才停止加热 | |
| B. | 蒸馏时,温度计水银球应靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色 |
分析 A.蒸发时,利用余热加热,不能蒸干;
B.蒸馏时,温度计测定馏分的温度;
C.分液时避免上下层液体混合;
D.稀硫酸不挥发,干扰实验.
解答 解:A.蒸发时,利用余热加热,不能蒸干,则蒸发皿中出现大量固体时才停止加热,故A正确;
B.蒸馏时,温度计测定馏分的温度,则温度计水银球应靠近蒸馏烧瓶的支管口处,故B正确;
C.分液时避免上下层液体混合,则分液漏斗中下层液体从下口放出,上层液体从上口倒出,故C正确;
D.稀硫酸不挥发,干扰实验,应选稀盐酸洗净铂丝,并在火焰上灼烧至无色,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、焰色反应、实验基本操作等为解答该题的关键,侧重分析与实验能力的考查,注意实验的评价性分析,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
11.下列说法正确的是( )
| A. | 离子化合物的熔点一定比共价化合物熔点高 | |
| B. | 甲烷的标准燃烧热为890.3KJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的△H相同 |
12.下列物质中属于天然高分子化合物的是( )
| A. | 乙酸 | B. | 葡萄糖 | C. | 淀粉 | D. | 维生素 |
9.关于下列各图的叙述不正确的是( )
| A. | 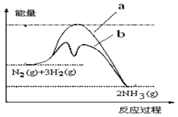 图中曲线b表示工业合成氨中加入铁触媒(催化剂)的能量变化曲线 | |
| B. | 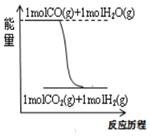 根据图可知在该条件下:CO2(g)+H2(g)═CO(g)+H2O(g)△H<0 | |
| C. |  图中曲线表示向1.0 mol•L-1的醋酸溶液中通入氨气,溶液导电能力的变化情况 | |
| D. |  图中曲线表示常温下向弱酸HA的稀溶液中加水稀释时,c(HA)/c(A-)的变化情况 |
6.下列物质的俗名与化学式相对应的是( )
| A. | 生石灰-Ca(OH)2 | B. | 石膏-Na2SO4•10H2O | ||
| C. | 水玻璃-Na2SiO3水溶液 | D. | 纯碱-NaOH |
13.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14.X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族.错误的是( )
| A. | 原子半径:r(Y)<r(Z) | |
| B. | X和Z都只能形成一种氧化物 | |
| C. | W的最高价氧化物对应的水化物是强酸 | |
| D. | Y的简单气态氢化物的热稳定性比W的强 |
10.“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请回答下列问题:
Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2.
Ⅱ、某稻壳灰的成分为:
通过如图流程可由稻壳灰制备较纯净的二氧化硅.
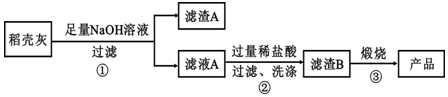
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三角架.
Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2.
Ⅱ、某稻壳灰的成分为:
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三角架.