题目内容
13.设阿伏加德罗常数为NA,则下列说法正确的是( )| A. | 甲烷的摩尔质量为16克 | |
| B. | 标准状况下,0.3molSO2中含氧原子数为0.3NA | |
| C. | 常温下,9.5克MgCl2晶体中含Mg2+为0.1 NA | |
| D. | 标准状况下,22.4L H2O含10 NA个电子 |
分析 A.摩尔质量单位为g/mol;
B.1个二氧化硫含有2个O;
C.依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算;
D.气体摩尔体积使用对象为气体.
解答 解:A.甲烷的摩尔质量为16g/mol,故A错误;
B.标准状况下,0.3molSO2中含氧原子数为0.3×2=0.6NA,故B错误;
C.常温下,9.5克MgCl2晶体中含Mg2+为:$\frac{9.5g}{95g/mol}$×1×NA=0.1 NA,故C正确;
D.标况下水是液态,不能使用气体摩尔体积,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析应用微粒个数计算,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
3. 2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因.
2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)△H<0.在一定温度下,在一个体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态.
①能判断该反应达到平衡状态的标志是CD.
A.在单位时间内生成1mol CO2的同时消耗了lmol CO
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再变化
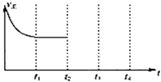
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件.请在图中补充画出从t2到t4时刻正反应速随时间的变化曲线:
③若要同时提高该反应的速率和NO的转化率,采取的措施有增大压强、增大CO浓度.(写出2个)
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,其反应C(g)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
①该反应在高温下能自发进行(填“高温”或“低温”).
②煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-.[已知:Ka1(H2S)=9.1×10-8,Ka2(H2S)=1.1×10-12;Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11]
(3)已知反应:CO(g)+H2O(g)?CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
①实验1条件下平衡常数K=2.67(保留小数点后二位).
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是a<b.
③该反应的△H>0 (填“<”或“>”);若在900℃时,另做一组实验,在此容器中加入l0mol CO、5mo1H2O、2mo1CO2、5mol H2,则此时v(正)<v(逆)(填“<”、“>”或“=”).
 2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因.
2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因.(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)△H<0.在一定温度下,在一个体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态.
①能判断该反应达到平衡状态的标志是CD.
A.在单位时间内生成1mol CO2的同时消耗了lmol CO
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再变化
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件.请在图中补充画出从t2到t4时刻正反应速随时间的变化曲线:
③若要同时提高该反应的速率和NO的转化率,采取的措施有增大压强、增大CO浓度.(写出2个)
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,其反应C(g)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
①该反应在高温下能自发进行(填“高温”或“低温”).
②煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-.[已知:Ka1(H2S)=9.1×10-8,Ka2(H2S)=1.1×10-12;Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11]
(3)已知反应:CO(g)+H2O(g)?CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需的时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是a<b.
③该反应的△H>0 (填“<”或“>”);若在900℃时,另做一组实验,在此容器中加入l0mol CO、5mo1H2O、2mo1CO2、5mol H2,则此时v(正)<v(逆)(填“<”、“>”或“=”).
8.在2L密闭容器内,加入0.100molCO气体和0.080molCuO固体,800℃时发生如下反应:2CuO(s)+CO(g)?Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
(1)用CO表示前2min内的化学反应速率=0.005mol/(L.min)
(2)计算此反应在800°C时的化学平衡常数k=0.429
(3)若向平衡后的体系中加入CO和CO2各0.05mol,则此时V(正)<V(逆)
(4)用来还原CuO的CO可以用C和水蒸气反应制得.
已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol
则C(s)+H2O(g)?CO(g)+H2(g)△H=+175.3kj/mol.
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(2)计算此反应在800°C时的化学平衡常数k=0.429
(3)若向平衡后的体系中加入CO和CO2各0.05mol,则此时V(正)<V(逆)
(4)用来还原CuO的CO可以用C和水蒸气反应制得.
已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol
则C(s)+H2O(g)?CO(g)+H2(g)△H=+175.3kj/mol.
18.同温同压下,已知O2的密度为ρg/L,则NH3的密度为( )
| A. | $\frac{32p}{17}$ g/L | B. | $\frac{17p}{32}$ g/L | C. | $\frac{32}{17p}$ g/L | D. | $\frac{17}{32p}$ g/L |
5.下列物质形成水溶液,溶液呈中性的是( )
| A. | CH3COONa | B. | NH4Cl | C. | KNO3 | D. | H2S |
3.表格中各项分类都正确的一组是( )
| 类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 苏打 | 纯净空气 | CaCO3 | 干冰 |
| B | 碘酒 | 漂白粉 | NH3•H20 | Fe |
| C | 明矾 | 铝合金 | 石墨 | 醋酸 |
| D | 盐酸 | CuSO4•5H2O | Na2SO4 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |