题目内容
3.表格中各项分类都正确的一组是( )| 类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 苏打 | 纯净空气 | CaCO3 | 干冰 |
| B | 碘酒 | 漂白粉 | NH3•H20 | Fe |
| C | 明矾 | 铝合金 | 石墨 | 醋酸 |
| D | 盐酸 | CuSO4•5H2O | Na2SO4 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
分析 纯净物是由一种物质组成的物质;
混合物由两种或两种以上物质组成;
在水溶液里或熔融状态下能导电的化合物是电解质;
在水溶液里或熔融状态下都不导电的化合物是非电解质.
解答 解:A.苏打是碳酸钠一种物质组成的纯净物,纯净空气是多种物质组成的混合物,碳酸钙熔融状态下导电属于电解质,干冰不能电离属于非电解质,故A正确;
B.碘酒是碘单质的酒精溶液,属于混合物,漂白粉是氯化钙和次氯酸钙的混合物,一水合氨能电离导电属于电解质,铁为单质既不是电解质也不是非电解质,故B错误;
C.明矾是一种物质组成的为纯净物,铝合金是多种物质组成的为混合物,石墨为单质既不是电解质也不是非电解质,醋酸为电解质,故C错误;
D.盐酸是氯化氢的水溶液属于混合物,硫酸铜晶体一种物质组成的为纯净物,硫酸钠溶于水溶液导电属于电解质,酒精不能电离属于非电解质,故D错误;
故选A.
点评 本题考查了纯净物、混合物、电解质和非电解质的判断,题目难度不大,明确能导电的不一定是电解质,电解质不一定导电.

练习册系列答案
相关题目
13.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 甲烷的摩尔质量为16克 | |
| B. | 标准状况下,0.3molSO2中含氧原子数为0.3NA | |
| C. | 常温下,9.5克MgCl2晶体中含Mg2+为0.1 NA | |
| D. | 标准状况下,22.4L H2O含10 NA个电子 |
14.在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的( )
| A. | 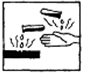 | B. |  | C. |  | D. |  |
11.下列除杂方法不正确的是( )
| A. | 除去NH4Cl溶液中的FeCl3,可向溶液中加入氨水调节pH | |
| B. | 除去金属离子Cu2+、Hg2+,可向溶液中加入H2S、Na2S等沉淀剂 | |
| C. | 除去某溶液中的SO42-可向溶液中加入镁盐 | |
| D. | 除去ZnCl2溶液中的Fe3+可向溶液中加入ZnO |
8.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,2.24 L CHCl3的原子总数为0.1 NA | |
| B. | 1 mol-OH中电子数为10 NA | |
| C. | 4.2 g C3H6中含有的碳碳双键数一定为0.1 NA | |
| D. | 常温常压下,28 g丙烯和丁烯的混合气体中含有的碳原子数为2 NA |
 .
.