题目内容
19.下列关于卤代烃的叙述错误的是( )| A. | 随着碳原子数的增多,一氯代烃的沸点逐渐升高 | |
| B. | 随着碳原子数的增多,一氯代烃的密度逐渐增大 | |
| C. | 等碳原子数的一氯代烃,支链越多,沸点越低 | |
| D. | 等碳原子数的一卤代烃,卤素的原子序数越大,沸点越高 |
分析 A、碳原子数越多,一氯代烃的相对分子质量越大,从而影响到分子间作用力;
B、碳原子数越多,一氯代烃的相对分子质量越大,从而影响到密度大小;
C、等碳原子数的一氯代烃,支链越多,则挥发越容易;
D、氟代烃分子间会存在氢键.
解答 解:A、碳原子数越多,一氯代烃的相对分子质量越大,从而分子间作用力越大,则沸点越高,故A正确;
B、碳原子数越多,一氯代烃的相对分子质量越大,则密度越大,故B正确;
C、等碳原子数的一氯代烃,支链越多,则挥发越容易,即沸点越低,故C正确;
D、氟代烃分子间会存在氢键,故一氟代烃是一卤代烃中沸点最高的,即并不是卤素原子的序数越大,沸点越高,故D错误.
故选D.
点评 本题考查了卤代烃的物理性质随着碳原子数的递增或卤素原子序数的递增而递变的规律,难度不大,应注意氢键的存在对沸点的影响.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
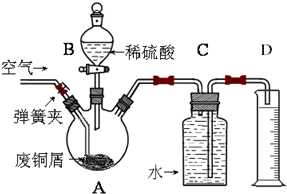
9.下列有关实验装置的说法,正确的是( )
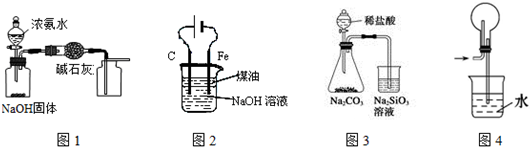

| A. | 用图1装置制取干燥纯净的NH3 | |
| B. | 用图2装置制备Fe(OH)2并能较长时间观察其颜色 | |
| C. | 装置3可证明非金属性Cl>C>Si | |
| D. | 装置4用于HCl的吸收,防止倒吸 |
7.短周期元素X、Y、Z、W、M的原子序数依次增大,且原子最外层电子数之和为17,X与Y是组成化合物种类最多的元素,W是地壳中含量最高的元素.下列说法正确的是( )
| A. | 原子半径大小顺序:r(Y)>r(Z)>r(W)>r(M) | |
| B. | 由三种元素X、Z、W形成的化合物中只有共价键而无离子键 | |
| C. | Z的气态氢化物比W的气态氢化物更稳定 | |
| D. | 分子式为Y4X8W2的物质超过10种 |
14.铯和钠都是第ⅠA族元素,以下关于铯的叙述,正确的是( )
| A. | 铯的密度比钠大,熔点比钠高 | |
| B. | 氢氧化铯易溶于水 | |
| C. | 铯能与热水反应放出氢气,但与冷水不反应 | |
| D. | 铯与氯形成共价化合物 |
5.用石墨作电极,电解质溶液中各离子浓度之比如下:c(Cu2+):c(Na+):c(Cl-)=1:2:4.在任何情况下,阴阳两极不可能同时发生的反应是( )
| A. | 阴极:2H++2e-═H2↑ 阳极:4OH--4e-═O2↑+2H2O | |
| B. | 阴极:Cu2++2e-═Cu 阳极:4OH--4e-═O2↑+2H2O | |
| C. | 阴极:2H++2e-═H2↑ 阳极:2C1--2e-═Cl2↑ | |
| D. | 阴极:Cu2++2e-═Cu 阳极:2C1--2e-═Cl2↑ |
 过硫酸:
过硫酸: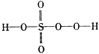
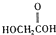 (b)
(b)  (c) H2O2 (d)
(c) H2O2 (d) 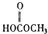
 (f)
(f)  (g) O2 (h)
(g) O2 (h) 

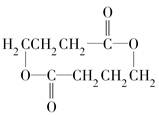 ;
;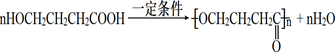 或
或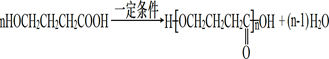 .
.