题目内容
9.下列说法正确的是( )| A. | 用pH试纸测氯水的pH | |
| B. | 保存液溴时液面覆盖一层水,并装在带玻璃塞的试剂瓶中 | |
| C. | 用稀盐酸清洗做过银镜反应的试管内壁 | |
| D. | 除去NaBr溶液中的NaI,可先加氯水,再用CCl4萃取分液 |
分析 A.氯气与水反应,发生Cl2+H2O=H++Cl-+HClO,氯水中含有HClO、Cl2,具有氧化性;
B.溴单质具有挥发性,需要用水液封,防止挥发,且溴能够氧化胶塞,应该用玻璃塞;
C.盐酸不与银单质反应,应该用稀硝酸清洗;
D.氯气能够以后溴离子和碘离子,应该用溴单质氧化.
解答 解:A.氯气可与水反应生成盐酸和次氯酸,其中盐酸可使pH变成红色,次氯酸具有强氧化性,可漂白试纸,最后使试纸变成白色,所以无法用PH试纸测氯水的PH值,故A错误;
B.保存液溴时液面覆盖一层水,可防止液溴挥发,另外溴具有强氧化性,不能使用胶塞,可装在带玻璃塞的试剂瓶中,故B正确;
C.由于稀盐酸不与银反应,无法洗去银单质,可用稀硝酸洗去,故C错误;
D.氯水能够将溴化钠氧化,应该用溴水,故D错误;
故选B.
点评 本题考查滴定操作方法、除杂方法、试剂的存放等知识,题目难度不大,明确常见物质的性质为解答关键,注意掌握pH试纸的使用方法、常见试剂的保存方法,试题培养了学生的灵活应用能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
19.下列反应的离子方程式书写正确的是( )
| A. | 将铁粉加入稀硫酸反中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将铜屑加入氯化铁溶液中:Fe3++Cu═Cu2++Fe2+ | |
| C. | 将过量的石灰水加入小苏打溶液中:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | 将氢氧化钡溶液滴加入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
17.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式为NaAl(OH)2CO3.关于该物质的说法正确的是( )
| A. | 该物质属于氢氧化物 | |
| B. | 该物质的摩尔质量是160g•mol-1 | |
| C. | 该物质的碱性不强 | |
| D. | 将1molNaAl(OH)2CO3溶于足量1mol•L-1HCl中时,共收集到2.5molCO2 |
4.分子式为C10H12O2的有机物,其苯环上只有两个取代基,且能与NaHCO3,溶液反应产生气体的结构(不是立体异构)有( )
| A. | 9种 | B. | 12种 | C. | 15种 | D. | 18种 |
16.火箭升空使用肼(N2H4)作为燃料,N2O4为氧化剂.
(1)已知:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ•mol-1
2NO2(g)?N2O4(g)△H=-52.7kJ•mol-1,气态肼在N2O4中燃烧生成氮气和水蒸气的热化学方程式为
2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1083.0kJ•mol-1.
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的化学方程式为NaClO+2NH3=NaCl+N2H4+H2O.
(3)一定条件下,向2L密闭容器中充入3.2mol NH3和4.4mol O2,发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0.测得平衡时数据如表所示:
①T1℃时,若经过10min反应达到平衡,则10min内反应的平均速率v(NH3)=0.08mol•L-1•min-1,该反应的化学平衡常数K=1.2.
②T1< T2 (填“>”、“<”或“=”).
③下列措施中,既能提高NH3的转化率,又能加快反应速率的是d(填选项字母).
a.升高温度 b.降低温度 c.扩大容器体积 d.体积不变的条件下再充入一定量O2
(4)在载人航天器的生态系统中,可利用电化学装置发生反应“2CO2═2CO+O2”分解除去CO2并提供充足的O2.已知该反应的阳极反应式为4OH--4e-═2H2O+O2↑,则阴极反应式为2CO2+4e-+2H2O=2CO+4OH-.有人提出,可以设计反应“2CO(g)=2C(s)+O2(g)△H>0”来消除CO的污染,请判断上述设计是否合理否(填“是”或“否”),理由是该反应为△H>0、△S<0的反应,不能自发进行.
(1)已知:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ•mol-1
2NO2(g)?N2O4(g)△H=-52.7kJ•mol-1,气态肼在N2O4中燃烧生成氮气和水蒸气的热化学方程式为
2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1083.0kJ•mol-1.
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的化学方程式为NaClO+2NH3=NaCl+N2H4+H2O.
(3)一定条件下,向2L密闭容器中充入3.2mol NH3和4.4mol O2,发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0.测得平衡时数据如表所示:
物质 物质的量/mol 温度/℃ | NO | H2O |
| T1 | 1.6 | 2.4 |
| T2 | 1.2 | 1.8 |
②T1< T2 (填“>”、“<”或“=”).
③下列措施中,既能提高NH3的转化率,又能加快反应速率的是d(填选项字母).
a.升高温度 b.降低温度 c.扩大容器体积 d.体积不变的条件下再充入一定量O2
(4)在载人航天器的生态系统中,可利用电化学装置发生反应“2CO2═2CO+O2”分解除去CO2并提供充足的O2.已知该反应的阳极反应式为4OH--4e-═2H2O+O2↑,则阴极反应式为2CO2+4e-+2H2O=2CO+4OH-.有人提出,可以设计反应“2CO(g)=2C(s)+O2(g)△H>0”来消除CO的污染,请判断上述设计是否合理否(填“是”或“否”),理由是该反应为△H>0、△S<0的反应,不能自发进行.
17.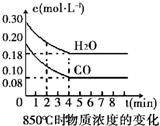 在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
①表中3min-4min之间反应处于平衡状态;C1数值大于0.08mol/L (填大于、小于或等于).
②反应在4min-5min问,平衡向逆方向移动,可能的原因是d(单选),表中5min-6min之间数值发生变化,可能的原因是a(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4min-5min问,平衡向逆方向移动,可能的原因是d(单选),表中5min-6min之间数值发生变化,可能的原因是a(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.