题目内容
【题目】(1)现有![]() 某气体(由双原子分子构成),其摩尔质量为
某气体(由双原子分子构成),其摩尔质量为![]() ,阿伏加德罗常数用
,阿伏加德罗常数用![]() 表示,试求
表示,试求
①该气体在标准状况下的体积为____![]() 。
。
②该气体所含原子数为____。
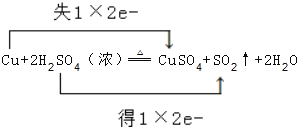
(2)用双线桥表示铜与浓硫酸反应的电子转移方向和数目:__________________

当有![]() 被还原时,转移电子的物质的量为____
被还原时,转移电子的物质的量为____![]() ,生成标准状况下
,生成标准状况下![]() 的体积为___
的体积为___![]() 。
。
【答案】![]() ×22.4
×22.4 ![]()
 2 22.4
2 22.4
【解析】
(1)根据n=![]() =
=![]() =
=![]() ;
;
(2)根据化合价的变化,用双线桥的箭头由氧化剂指向还原产物,由还原剂指向氧化产物,根据化合价的变化,找到转移的电子数,生成二氧化硫的物质的量,由n=![]() ,得到二氧化硫的体积;
,得到二氧化硫的体积;
(1)m g某气体的物质的量为n=![]() =
=![]() mol,该气体在标准状况下的体积为V=nVm=
mol,该气体在标准状况下的体积为V=nVm=![]() ×22.4L;
×22.4L;
所含气体的分子数N=nNA=![]() ×NA mol,该分子是双原子分子,故原子数为
×NA mol,该分子是双原子分子,故原子数为![]() ×NA×2=
×NA×2=![]() ;
;
(2)由于铜的化合价升高了2,硫的化合价降低了2,所以该反应转移2mol电子,表示方法为: ;当有2mol硫酸参加反应,被还原的硫酸为1mol,转移电子的物质的量为2mol电子,生成
;当有2mol硫酸参加反应,被还原的硫酸为1mol,转移电子的物质的量为2mol电子,生成![]() 1mol;所以则当有
1mol;所以则当有![]() 被还原时,转移电子的物质的量为2mol,生成
被还原时,转移电子的物质的量为2mol,生成![]() 为1mol,在标况下的体积为V=nVm=1mol×22.4L/mol=22.4L。
为1mol,在标况下的体积为V=nVm=1mol×22.4L/mol=22.4L。

练习册系列答案
相关题目