题目内容
17.化学是你,化学是我,说明了化学知识在生活中的普遍性.下列有关说法正确的是( )| A. | “洁厕灵”有效成分为盐酸,与漂白液的成分相同 | |
| B. | 静置后的淘米水能产生丁达尔效应,这种“淘米水”是胶体 | |
| C. | 生物油和矿物油均可发生水解反应 | |
| D. | 铁粉可用作食品干燥剂 |
分析 A.洁厕灵”有效成分为盐酸,而漂白液的成分为NaClO;
B.丁达尔效应为胶体特有的性质;
C.矿物油为烃类物质;
D.铁具有还原性,不能吸水.
解答 解:A.洁厕灵”有效成分为盐酸,而漂白液的成分为NaClO,二者成分不同,且不同混合使用,故A错误;
B.丁达尔效应为胶体特有的性质,则静置后的淘米水能产生丁达尔效应,这种“淘米水”是胶体,故B正确;
C.矿物油为烃类物质,不能水解,而油脂能水解,故C错误;
D.铁具有还原性,不能吸水,则不能作干燥剂,可作抗氧化剂,故D错误;
故选B.
点评 本题考查物质的性质与应用,为基础性习题,把握物质的组成、性质、应用为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
7.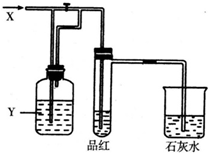 如图所示是一套检验气体性质的实验装置.向装置中缓慢加入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
如图所示是一套检验气体性质的实验装置.向装置中缓慢加入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
 如图所示是一套检验气体性质的实验装置.向装置中缓慢加入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
如图所示是一套检验气体性质的实验装置.向装置中缓慢加入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )| ① | ② | ③ | ④ | |
| X | SO2 | H2S | CO2 | Cl2 |
| Y | 饱和的NaHCO3溶液 | 浓硫酸 | Na2SO3溶液 | Na2CO3溶液 |
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
8.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如下:
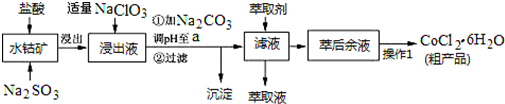
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3.
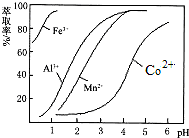
(4)萃取剂对金属离子的萃取率与pH的关系如图.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
5.某课外活动小组,收集了一种合金进行研究:
(1)外观暗灰色,表皮光滑.
(2)在酒精灯上灼烧,火焰绿色;合金片熔化,但不滴落.
(3)取刮去表皮的金属,放入足量稀硫酸中,收集到标准状况下氢气9.96 L.
(4)另取刮去表皮的金属,放入足量氢氧化钠溶液中,也收集到标准状况下氢气9.96 L.
试据此判断,合金中含有的成分是( )
(1)外观暗灰色,表皮光滑.
(2)在酒精灯上灼烧,火焰绿色;合金片熔化,但不滴落.
(3)取刮去表皮的金属,放入足量稀硫酸中,收集到标准状况下氢气9.96 L.
(4)另取刮去表皮的金属,放入足量氢氧化钠溶液中,也收集到标准状况下氢气9.96 L.
试据此判断,合金中含有的成分是( )
| A. | Cu、Fe | B. | K、Na | C. | Cu、Al | D. | Zn、Mg |
12.某离子化合物中,阳离子和阴离子的电子层结构与氖原子电子层结构相同,则此离子化合物化学式为( )
| A. | MgCl2 | B. | NaF | C. | MgO | D. | K2S |
2.用下列试剂或方法不能鉴别NaCl溶液和KOH溶液的是( )
| A. | 无色酚酞试液 | B. | Ba(NO3)2溶液 | C. | CuCl2溶液 | D. | 焰色反应 |
3.下列仪器:①漏斗 ②容量瓶 ③蒸馏烧瓶 ④坩埚⑤分液漏斗⑥燃烧匙常用于物质分离的是( )
| A. | ①③④ | B. | ①②⑥ | C. | ①③⑤ | D. | ③⑤⑥ |