题目内容
18.下列对氯及其化合物的说法正确的是( )| A. | 少量的铁在氯气中燃烧生成FeCl3,过量的铁在氯气中燃烧生成FeCl2 | |
| B. | 用pH试纸可测得氯水的pH值 | |
| C. | 溴化钠溶液中加入少量新制氯水振荡,再加入少量四氯化碳振荡,静置后,上层颜色变浅,下层颜色变橙红色 | |
| D. | 由Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO,可推出Ca(ClO)2+SO2+H2O═CaCO3↓+2HClO |
分析 A.氯气具有强氧化性,铁和氯气反应生成氯化铁,与铁的量多量少无关;
B.氯水中次氯酸具有漂白性;
C.溴化钠溶液中加入少量新制氯水,发生氧化还原反应生成溴,萃取后在下层;
D.Ca(ClO)2+CO2+H2O═CaCO3+2HClO为强酸制取弱酸的反应,而Ca(ClO)2+SO2+H2O应发生氧化还原反应.
解答 解:A.氯气具有强氧化性,则过量的铁在氯气中燃烧可生成氯化铁,故A错误;
B.氯水中含HClO,具有漂白性,不能利用pH试纸测定氯水的pH,应利用pH计,故B错误;
C.溴化钠溶液中加入少量新制氯水,发生氧化还原反应生成溴,再加入少量四氯化碳振荡,静置后,上层颜色变浅,下层颜色变橙红色,故C正确;
D.Ca(ClO)2+CO2+H2O═CaCO3+2HClO为强酸制取弱酸的反应,而Ca(ClO)2+SO2+H2O应发生氧化还原反应生成硫酸钙和盐酸,故D错误;
故选C.
点评 本题考查氯气及其化合物的性质,涉及氧化还原反应、pH的测定、萃取及反应原理等,为常见的小综合习题,注重基础知识的考查,题目难度中等.

练习册系列答案
相关题目
8.胶体最本质的特征是( )
| A. | 丁达尔效应 | |
| B. | 可以通过滤纸 | |
| C. | 布朗运动 | |
| D. | 分散质粒子的直径在10-9~10-7 m之间 |
6.某溶液中有NH4+、Fe3+、Al3+和Cl-四种离子,若向其中加入过量的NaOH溶液,微热拌搅拌,再加入过量的盐酸,溶液中大量减少的离子是( )
| A. | Cl- | B. | Al3+ | C. | Fe3+ | D. | NH${\;}_{4}^{+}$ |
13.下列溶液中,溶质的物质的量浓度为0.1mol/L的是( )
| A. | 将4gNaOH溶液溶入1L水中 | |
| B. | 常温下,将2.24LHCl气体溶于水配成1L溶液 | |
| C. | 含有4.9gH2SO4的溶液500mL | |
| D. | 将6.2gNa2O溶于水配成1L溶液 |
3.下列说法正确的是( )
| A. | 胶体的本质特征是丁达尔效应 | |
| B. | 胶体的介稳性在生产和生活中应用比较普遍,如颜料、墨水的制造,洗涤剂、喷雾剂的应用等 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 金属氧化物一定是碱性氧化物 |
8.下列指定反应的离子方程式正确的是( )
| A. | 将铜插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O═Al(OH)3↓+3NH4+ | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
 ;
;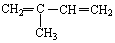 与Br2按物质的量之比1:1发生1,4加成反应方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br
与Br2按物质的量之比1:1发生1,4加成反应方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br