题目内容
18.下列属于电解质是( )| A. | 淀粉 | B. | KNO3溶液 | C. | 乙醇 | D. | 熔融的NaCl |
分析 电解质是在水溶液中或熔融状态下能导电的化合物,据此分析.
解答 解:A、淀粉在水溶液中和熔融状态下均不导电,故为非电解质,故A错误;
B、硝酸钾溶液为混合物,故既不是电解质也不是非电解质,故B错误;
C、乙醇在水溶液中和熔融状态下均不导电,故为非电解质,故C错误;
D、熔融氯化钠即液态的氯化钠,在水溶液中和熔融状态下均能导电,故为电解质,故D正确.
故选D.
点评 本题考查了电解质的判断和概念,难度不大,根据定义来分析即可.

练习册系列答案
相关题目
8.有一水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:(注:已知NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O)
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.04mol气体;
第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g
综合上述实验,你认为以下结论正确的是( )
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.04mol气体;
第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g
综合上述实验,你认为以下结论正确的是( )
| A. | 加入AgNO3溶液后生成的沉淀一定是AgCl | |
| B. | 该混合液中-定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 该混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+ | |
| D. | 该混合液中:c(K+)≥0.2mol/L c(CO32-)=0.2mol/L |
9.下列叙述中正确的是( )
| A. | 1mol H2O的质量为18g•mol-1 | |
| B. | CO2的摩尔质量为44g | |
| C. | 1mol任何物质的质量等于该物质的相对分子质量 | |
| D. | H+的摩尔质量为1g•mol-1 |
6.氢氰酸(HCN)的下列性质中,不能证明它是弱电解质的是( )
| A. | HCN溶液的导电性比盐酸的弱 | B. | 1mol/LNaCN溶液呈碱性 | ||
| C. | NaCN可以与盐酸反应 | D. | 1mol/LHCN溶液的pH约为3 |
13.下列各种维生素或微量元素与其缺乏症之间不对应的是( )
| A. | 缺维生素A易患夜盲症 | B. | 缺铁易患白血病 | ||
| C. | 缺维生素C易患坏血病 | D. | 缺维生素D易患佝偻病 |
 用下列装置制取并收集纯净的氯气,试回答下列问题:
用下列装置制取并收集纯净的氯气,试回答下列问题: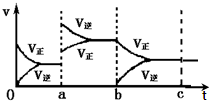 如图表示在密闭容器中反应:2SO2+O2?2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是升温;bc过程与ab过程相比化学平衡常数不变.(填“增大”“减小”或“不变”)
如图表示在密闭容器中反应:2SO2+O2?2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是升温;bc过程与ab过程相比化学平衡常数不变.(填“增大”“减小”或“不变”)