题目内容
【题目】常温下,下列有关电解质溶液的说法正确的是( )
A.0.2 mo1CO2通入1L 0.3molL-1 KOH溶液中:2c(H+)+c(HCO3-)+3c(H2CO3)=2c(OH-)+c(CO32-)
B.Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
C.常温下pH=4.75、浓度均为0.1mol/L 的CH3COOH、CH3COONa 混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
D.已知一定浓度的NaHSO3溶液pH=5.4,则c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)
【答案】A
【解析】
A项,0.2 mo1CO2通入1L 0.3molL-1 KOH溶液中,反应后溶质为等浓度的碳酸钾、碳酸氢钾,根据电荷守恒可知:![]() ,根据溶液中物料守恒得到:
,根据溶液中物料守恒得到:![]() ,将两式整理可得:2c(H+)+c(HCO3-)+3c(H2CO3)=2c(OH-)+c(CO32-),故A项正确;
,将两式整理可得:2c(H+)+c(HCO3-)+3c(H2CO3)=2c(OH-)+c(CO32-),故A项正确;
B项,在Na2CO3溶液中存在物料守恒,![]() ,故B项错误;
,故B项错误;
C项,pH=4.75浓度均为0.1mol/L 的CH3COOH、CH3COONa 混合溶液,说明醋酸的电离程度大于醋酸根的水解程度,则:![]() ,根据电荷守恒
,根据电荷守恒![]() 可知:
可知:![]() ,故C项错误;
,故C项错误;
D项,一定浓度的NaHSO3溶液pH=5.4,说明亚硫酸氢根的电离程度大于其水解程度,则![]() ,溶液中正确的离子浓度大小为:
,溶液中正确的离子浓度大小为:![]() ,故D项错误。
,故D项错误。
综上所述,本题正确答案为A。

 阅读快车系列答案
阅读快车系列答案【题目】为探究化学反应“2Fe3++2I-2Fe2++I2”存在限度及平衡移动与物质的浓度、性质的关系,甲、乙两同学进行如下实验。
已知:a.含I2的溶液呈黄色或棕黄色。b.利用色度计可测定溶液的透光率,通常溶液颜色越深,透光率数值越小。
Ⅰ.甲同学设计下列实验进行相关探究,实验如下:

回答下列问题:
(1)甲同学利用实验②中i和ii证明Fe2(SO4)3溶液与KI溶液的反应存在限度,实验i中的现象是________,实验ii中a是________(化学式)溶液。
(2)用离子方程式表示实验②iii中产生黄色沉淀的原因________。
Ⅱ.乙同学:利用色度计对Fe2(SO4)3溶液与KI溶液的反应进行再次探究
(实验过程)
序号 | 实验步骤1 | 实验步骤2 |
实验③ | 将盛有2mL蒸馏水的比色皿放入色度计的槽孔中 | 向比色皿中逐滴滴入5滴(每滴约0.025mL)0.05mol·L-1Fe2(SO4)3溶液,同时采集溶液的透光率数据 |
实验④ | 将盛有2mL0.1mol·L-1KI溶液的比色皿放入色度计的槽孔中 | 同上 |
实验⑤ | 将盛有2mL0.2mol·L-1KI溶液的比色皿放入色度计的槽孔中 | 同上 |
实验中溶液的透光率数据变化如图所示:

回答下列问题:
(3)乙同学实验③的目的是______。
(4)乙同学通过透光率变化推断:FeCl3溶液与KI溶液的反应存在限度。其相应的推理过程是______。
(5)乙同学根据氧化还原反应的规律,用如图装置(a、b均为石墨电极),探究化学平衡移动与I-与Fe2+浓度及还原性强弱关系,操作过程如下:

①K闭合时,电流计指针向右偏转,乙同学得出结论:2Fe3++2I—2Fe2++I2向正反应方向进行,b作______(填“正”或“负”)极,还原性I—>Fe2+。
②当指针归零(反应达到平衡)后,向U型管右管滴加0.1mol/LFeSO4溶液,电流计指针向左偏转,由此得出还原性Fe2+_____I—(填“>”或“<”)。
(6)综合甲、乙两位同学的实验探究过程,得出的结论有______。
【题目】![]() 与
与![]() 催化重整反应为
催化重整反应为![]()
![]() 。现向
。现向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() 和
和![]() 进行催化重整反应,不同温度下平衡体系中
进行催化重整反应,不同温度下平衡体系中![]() 和CO的体积分数
和CO的体积分数![]() 随温度变化如下表所示:
随温度变化如下表所示:
体积分数 温度 |
|
|
| a | a |
| c | b |
测得:![]() ,下列说法正确的是
,下列说法正确的是![]()
![]()
A.![]() 大于
大于![]()
B.![]() 时该反应的平衡常数为
时该反应的平衡常数为![]()
C.![]() 时向
时向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() 和
和![]() 进行催化重整反应,达到平衡时,
进行催化重整反应,达到平衡时,![]() 为
为![]()
D.![]() 时向
时向![]() 恒容密闭容器中充入等物质的量
恒容密闭容器中充入等物质的量![]() 、
、![]() 、CO、
、CO、![]() 进行催化重整反应,此时反应可能正向移动
进行催化重整反应,此时反应可能正向移动
【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
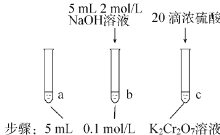
| 待试管b中颜色不变后与试管a比较,溶液颜色变浅。滴加浓硫酸,试管c温度略有升高,溶液颜色与试管 a 相比,变深。 |
已知:![]() (aq)(橙色) + H2O(l)2
(aq)(橙色) + H2O(l)2![]() (aq) (黄色)+ 2H+(aq) △H=+13.8 kJ/mol
(aq) (黄色)+ 2H+(aq) △H=+13.8 kJ/mol
A.该反应为氧化还原反应
B.待试管 b 中溶液颜色不变的目的是使![]() 完全反应
完全反应
C.试管c中的现象说明影响平衡的主要因素是温度
D.该实验不能证明减小生成物浓度平衡正向移动
【题目】一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)A(s)+B(g)![]() C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
Ⅲ | 0.32 | 1.0 | 0 | 0 | |
Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ
D.容器Ⅳ中c(D)= 0.4 mol·L-1