题目内容
5.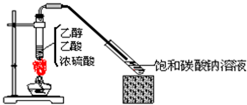 如图所示,实验室制乙酸乙酯1mL后,沿器壁加入紫色石蕊试液0.5mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间(整个过程不振荡).对可能出现的现象,叙述正确的是
如图所示,实验室制乙酸乙酯1mL后,沿器壁加入紫色石蕊试液0.5mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间(整个过程不振荡).对可能出现的现象,叙述正确的是( )
| A. | 石蕊层仍为紫色,有机层无色 | |
| B. | 石蕊层有两层,上层为紫色,下层为蓝色 | |
| C. | 石蕊层为三层环,由上而下是红、紫、蓝 | |
| D. | 石蕊层为三层环,由上而下是蓝、紫、红 |
分析 石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间,乙酸乙酯的密度比水的密度小,在最上层,结合碳酸钠溶液显碱性及指示剂的变色来解答.
解答 解:石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间,乙酸乙酯的密度比水的密度小,不溶于水,则石蕊层为三层环,
由上而下,混合液上层为乙酸乙酯中混有的乙酸,可使石蕊呈红色,
中层为紫色石蕊,所以颜色为紫色,
下层为碳酸钠溶液,碳酸根离子水解,溶液呈碱性,则溶液呈蓝色,
所以石蕊层为三层环,由上而下分别是:红、紫、蓝,
故选C.
点评 本题考查有机实验的评价,为高频考点,把握有机物的制备实验、乙酸乙酯中混有乙酸为解答的关键,侧重分析与应用能力的考查,注意指示剂的变色,题目难度不大.

练习册系列答案
相关题目
16.“碘钟”实验中,3I-(aq)+S2O82-(aq)?I3-(aq)+2SO42- (aq)的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,记录的数据如下表:
(1)写出反应的平衡常数表达式K=$\frac{c({{I}_{3}}^{-})•{c}^{2}(S{{O}_{4}}^{2-})}{{c}^{3}({I}^{-})•c({S}_{2}{{O}_{8}}^{2-})}$.
(2)反应中发生反应的I-与被氧化的I-的物质的量比为3:2.
(3)该实验的目的是研究I-、S2O82-浓度对反应速率的影响;显色时间t1=22s;若c(I-)=0.64mol/L,c(S2O82-)=0.02mol/L,请估算该反应显色的时间应为11s.
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c( S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
(2)反应中发生反应的I-与被氧化的I-的物质的量比为3:2.
(3)该实验的目的是研究I-、S2O82-浓度对反应速率的影响;显色时间t1=22s;若c(I-)=0.64mol/L,c(S2O82-)=0.02mol/L,请估算该反应显色的时间应为11s.
13.深红色气体氧化剂红氧的化学式为O8,在相同条件下,等物质的量的O8和O4具有相同的( )
| A. | 原子数 | B. | 质量 | C. | 密度 | D. | 分子数 |

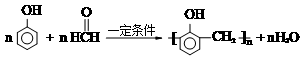 ,福尔马林是甲醛含量37%的水溶液,它的一个用途是浸制生物标本.
,福尔马林是甲醛含量37%的水溶液,它的一个用途是浸制生物标本.

