题目内容
9.1LMgCl2溶液中含Cl-6.02×1023个,则溶液的物质的量浓度是( )| A. | 0.5mol/L | B. | 1.0mol/L | C. | 1.5mol/L | D. | 3.0mol/L |
分析 根据n=$\frac{N}{{N}_{A}}$计算出该溶液中含有氯离子的物质的量,然后根据氯化镁的化学式计算出氯化镁的物质的量,最后根据c=$\frac{n}{V}$计算出该溶液的浓度.
解答 解:6.02×1023个Cl-的物质的量为:n(Cl-)=$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}}$mol=1mol,
根据化学式MgCl2可知,该溶液中氯化镁的物质的量为:n(MgCl2)=$\frac{1}{2}$n(Cl-)=1mol×$\frac{1}{2}$=0.5mol,
该溶液中氯化镁的物质的量浓度为:c(MgCl2)=$\frac{0.5mol}{1L}$=0.5mol/L,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意掌握物质的量与物质的量浓度、阿伏伽德罗常数之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
19.氮的氢化物NH3和N2H4有广泛应用.
(1)已知25℃时,几种难溶电解质的溶度积如下表所示:
向Cu2+、Mg2+、Fe3+、Fe2+浓度都为0.01mol•L-1的溶液中缓慢滴加稀氨水,产生沉淀的先后顺序为 (用化学式表示)Fe(OH)3、Cu(OH)2、Fe(OH)2、Mg(OH)2.
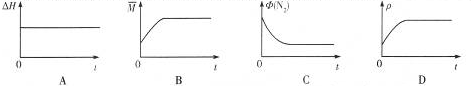
(2)实验室制备氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.工业上,制备肼(N2H4)的方法之一是用次氯酸钠溶液在碱性条件下与氨气反应.以石墨为电极,将该反应设计成原电池,该电池的负极反应为2NH3+2OH--2e-═N2H4+2H2O.
(3)在3L密闭容器中,起始投入4molN2和9molH2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1molN2(g)和3molH2(g)中的化学键消耗的总能量小于破坏2molNH3(g)中的化学键消耗的能量.
①则T1<T2(填“>”、“<”或“=”)
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1 mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.若再增加氢气浓度,该反应的平衡常数将不变(填“增大”、“减小”或“不变”)
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量( $\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是BC.
(1)已知25℃时,几种难溶电解质的溶度积如下表所示:
| 氢氧化物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| Ksp | 2.2×10-20 | 4.0×10-38 | 8.0×10-16 | 1.8×10-11 |
(2)实验室制备氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.工业上,制备肼(N2H4)的方法之一是用次氯酸钠溶液在碱性条件下与氨气反应.以石墨为电极,将该反应设计成原电池,该电池的负极反应为2NH3+2OH--2e-═N2H4+2H2O.
(3)在3L密闭容器中,起始投入4molN2和9molH2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1<T2(填“>”、“<”或“=”)
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1 mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.若再增加氢气浓度,该反应的平衡常数将不变(填“增大”、“减小”或“不变”)
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量( $\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

20.下列物质中属于有机物的是( )
| A. | 碳酸 | B. | 二氧化碳 | C. | 碳酸钠 | D. | 甲烷 |
17.下列反应中,生成的有机物只有一种的是( )
| A. | 异戊二烯(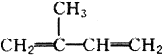 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷(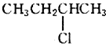 )与NaOH乙醇溶液共热发生消去HCl分子的反应 )与NaOH乙醇溶液共热发生消去HCl分子的反应 | |
| C. | 甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应 | |
| D. | 新戊烷和氯气发生取代反应生成一氯取代物的反应 |
4.下列溶液中的Cl-浓度与1mol/LMgCl2溶液中的Cl-浓度相等的是( )
| A. | 1mol/L NaCl溶液 | B. | 1 mol/LCaCl2溶液 | ||
| C. | 1 mol/L KCl溶液 | D. | 1 mol/LAlCl3溶液 |
18.符合如图阴影部分的物质是( )
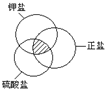

| A. | KHSO4 | B. | K2SO4 | C. | K2CO3 | D. | KAl(SO4)2•12H2O |
19.可逆反应mA(s)+nB(g)?cC(g)+dD(g) 反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )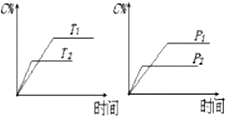

| A. | 达平衡后,加入催化剂则C%增大 | B. | 达平衡后,若升温,平衡左移 | ||
| C. | 化学方程式中n>c+d | D. | 达平衡后,增加A的量平衡向右移动 |