题目内容
10.某烷烃和烯烃的混合气体密度是1.07g/L(标况下),该烷烃和烯烃的体积比是4:1,则这两种烃是( )| A. | CH4 和 C2H4 | B. | C2H6和C2H4 | C. | CH4和C4H8 | D. | C2H4和 C3H6 |
分析 某烷烃和烯烃的混合气体的密度是1.07g/L(标准状况),则平均相对分子质量为1.07×22.4=24,由于烯烃中乙烯的相对分子质量最小为28,故含有的烷烃为甲烷,结合体积比计算烯烃的相对分子质量,进而确定烯烃的分子式.
解答 解:某烷烃和烯烃的混合气体的密度是1.07g/L(标准状况),则平均相对分子质量为1.07×22.4=24,由于烯烃中乙烯的相对分子质量最小为28,故含有的烷烃为甲烷,
假设烯烃相对分子质量为a,则$\frac{4×16+a}{4+1}$=24,解得a=56,
令烯烃组成为CnH2n,则14n=56,故n=4,则相同分子式为C4H8,
故选C.
点评 本题考查有机物推断,关键是利用平均相对分子质量确定含有甲烷,侧重考查学生分析计算能力.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
5.下列化合物中既能使溴的四氯化碳溶液褪色,又能在光照下与溴发生取代反应的是( )
| A. | 甲苯 | B. | 乙烷 | C. | 丙烯 | D. | 乙烯 |
1.A、B、C、D为四种短周期主族元素,且原子序数依次增大.已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子.下列说法不正确的是( )
| A. | 原子半径:C>D>A>B | |
| B. | A、C、D元素最高价氧化物的水化物间相互反应 | |
| C. | C、D、A、B四种元素的最高价化合价依次升高 | |
| D. | B元素在周期表中的位置为第二周第ⅥA族 |
18.不能将有机物鉴别开来的一组是( )
| A. | 用在空气中点燃的方法鉴别甲烷、乙烯和乙炔 | |
| B. | 用新制的氢氧化铜悬浊液鉴别乙酸、乙醇和乙醛三种液体 | |
| C. | 用酸性高锰酸钾溶液鉴别苯甲醇、苯酚、醛甲醛三种溶液 | |
| D. | 用溴水鉴别已烯、四氯化碳、乙苯三种溶液体 |
15.下列实验中均伴有颜色的变化,与其他颜色褪色原理不同的是( )
| A. | 臭氧使有色布条褪色 | B. | SO2使品红溶液褪色 | ||
| C. | 氯气使鲜花褪色 | D. | 过氧化钠使品红溶液褪色 |
2.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | HI气体受热分解 | C. | 食盐熔化 | D. | 金属钠熔化 |
19.已知短周期元素的离子,A2+,B+,C3-,D-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径A>B>D>C | B. | 原子序数D>C>B>A | ||
| C. | 离子半径C3->D->B+>A2+ | D. | 单质的还原性A>B>D>C |
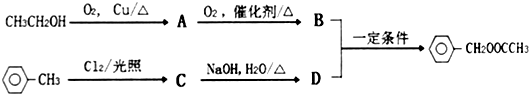
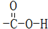 .
.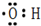 .
.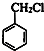 ,D的名称是苯甲醇.
,D的名称是苯甲醇. .
.