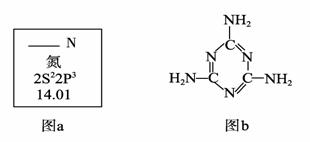
题目内容
下列是有关实验室制取乙炔的实验问题,按要求回答:(1)为了控制水与电石的反应速率并得到平稳的气流,用广口瓶和分液漏斗作反应容器时,采取的措施是_____________;用大试管作反应容器时,采取的措施是____________。
(2)用试管制取少量乙炔时,在试管上部放置一团疏松的棉花,其作用是____________。
(3)实验室制取下列气体时,不能使用启普发生器的是__________________。
A.用大理石和盐酸反应制CO2 B.用电石和水反应制C2H2
C.用锌粒和稀硫酸制H2 D.用亚硫酸钠和硫酸制SO2
解析:
| 解析:(1)用广口瓶和分液漏斗作反应器时,可用分液漏斗的活塞控制水的下滴速率,进而控制化学反应速率.用大试管作反应器时,可用饱和食盐水代替水,减少H2O与电石的接触,减缓反应速率.
(2)用试管作反应器制乙炔时,水(或饱和食盐水)一次性加入,与电石接触面积大,反应剧烈,产生大量的气体泡沫,而试管的容积又小,放置疏松的棉花,可防止泡沫从导管喷出. (3)对于B,反应生成的Ca(OH)2会堵塞反应容器,使水面难以升降,另外,此反应放出大量的热,会损坏启普发生器.对于D,亚硫酸钠为粉末状而非块状,且易溶于水,而生成的SO2极易溶于水.所以它们不可用启普发生器制取.
|

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某兴趣小组设计并进行了以下实验来探究Cl2、漂白粉的制备及有关性质。
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:
H→ 、 → 、 → ;广口瓶Ⅱ中的试剂为 。

(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:
;
某学生设计如下实验进一步探究SO2与漂粉精的反应:
|
操作 |
现象 |
|
取4 g漂粉精固体,加入100 mL水 |
部分固体溶解,溶液略有颜色 |
|
过滤,测漂粉精溶液的pH |
pH试纸先变蓝(约为12),后褪色 |
|
A |
ⅰ.液面上方出现雾状物 ⅱ.稍后,出现浑浊,溶液变为黄绿色 ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(3)pH试纸颜色的变化说明漂粉精溶液具有的性质是 。
(4)该同学推测现象i的雾状物由盐酸小液滴形成,进行如下实验加以进一步验证:
a.用湿润的碘化钾淀粉试纸检验雾状物,无变化;
b.搜集雾状物,用酸化的AgNO3溶液检验,产生白色沉淀。
实验a的目的是 。
(5)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的某些成份之间发生反应。请设计实验方案,进一步确认这种可能性,方案为
。
(6)用化学方程式解释现象ⅲ中黄绿色褪去的原因: 。检验褪色后溶液中是否有 的方法是:
。
的方法是:
。
二氯化二硫![]() 在工业上用于橡胶的硫化。为在实验室合成
在工业上用于橡胶的硫化。为在实验室合成![]() ,某化学研究性学习小组查阅了有关资料,得到如下信息:
,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在![]() 与硫反应,即可得
与硫反应,即可得![]() 粗品。
粗品。
②有关物质的部分性质如下表:
物质 | 熔点 | 沸点 | 化学性质 |
|
|
| 略 |
|
|
| 遇水生成 以上完全分解; |
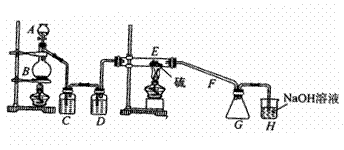 设计实验装置图如下:
设计实验装置图如下:
(1)图中气体发生和尾气处理装置不够完善,请提改进意见
。
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式: ;
E中反应的化学方程式: 。
(3)C、D中的试剂分别是 、 。
(4)如果在加热E时温度过高,对实验结果的影响是 ,在F中可能出现的现象是 。
(5)![]() 粗品中可能混有的杂质是(填写两种) 、 ,为了提高
粗品中可能混有的杂质是(填写两种) 、 ,为了提高![]() 的纯度,关键的操作是控制好温度和 。
的纯度,关键的操作是控制好温度和 。