题目内容
1.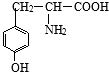 有一种结构简式如图的有机物,请回答下列问题:
有一种结构简式如图的有机物,请回答下列问题:①该有机物的分子式为C9H11O3N.
②该有机物与氢氧化钠溶液反应的化学方程为
 +2NaOH→
+2NaOH→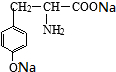 +2H2O.
+2H2O.
分析 根据结构简式确定有机物含有的元素种类和原子个数,可确定有机物分子式,有机物含有羧基和酚羟基,都可与氢氧化钠溶液反应,以此解答该题.
解答 解:(1)由结构简式可知有机物分子式为C9H11O3N,故答案为:C9H11O3N;
(2)有机物含有羧基和酚羟基,都可与氢氧化钠溶液反应,反应的方程式为 +2NaOH→
+2NaOH→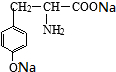 +2H2O,
+2H2O,
故答案为: +2NaOH→
+2NaOH→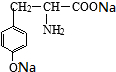 +2H2O.
+2H2O.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,题目难度不大.

练习册系列答案
相关题目
11.在标准状况下,进行甲、乙、丙三组实验:三组各取60mL 同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A. | 甲组和乙组的实验中,盐酸均是过量的 | |
| B. | 盐酸的物质的量浓度为0.8 mol/L | |
| C. | 合金中镁铝的物质的量之比为1:1 | |
| D. | 丙组充分反应后铝的物质的量为0.01mol |
12.下列物质之需克服范德华力,就可气化的是( )
| A. | 液态氮 | B. | 液态氟化氢 | C. | 液态氨 | D. | 干冰 |
13.水的电离过程为H2O?H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14.则下列叙述正确的是( )
| A. | c(H+)随温度的升高而降低 | |
| B. | 35℃时,c(H+)>c(OH-) | |
| C. | 溶液:pH(35℃)>pH(25℃) | |
| D. | 35℃时已电离的水的浓度约为2×10-7mol/L |
10.进行下列反应后,所得溶液中一定只含有一种溶质的是( )
| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入Na2CO3溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | 将CO2通入一定量的NaOH溶液中 |
9.一定温度下,向 a L密闭容器中加入1mol X 气体和2mol Y 气体,发生如下反应:X(g)+2Y(g)?3Z(g),此反应达到平衡的标志是( )
| A. | 容器内压强不再随时间变化 | |
| B. | 单位时间内消耗0.1 mol X 的同时生成0.3 molZ | |
| C. | 容器内XYZ的浓度比为1:2:3 | |
| D. | 容器内各物质浓度不再随时间变化 |