题目内容
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
| A、体积比1:1 |
| B、体积比16:11 |
| C、密度比16:11 |
| D、密度比11:16 |
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,Vm相同,结合n=
、V=nVm、ρ=
计算.
| m |
| M |
| M |
| Vm |
解答:
解:等质量的SO2和CO2,物质的量之比为
:
=11:16,则
A.同温同压下,Vm相同,体积之间等于物质的量之比,为11:16,故A错误;
B.同温同压下,Vm相同,体积之间等于物质的量之比,为11:16,故B错误;
C.相同条件下,密度之比等于摩尔质量之比,为64:44=16:11,故C正确;
D.相同条件下,密度之比等于摩尔质量之比,为64:44=16:11,故D错误;
故选C.
| m |
| 64 |
| m |
| 44 |
A.同温同压下,Vm相同,体积之间等于物质的量之比,为11:16,故A错误;
B.同温同压下,Vm相同,体积之间等于物质的量之比,为11:16,故B错误;
C.相同条件下,密度之比等于摩尔质量之比,为64:44=16:11,故C正确;
D.相同条件下,密度之比等于摩尔质量之比,为64:44=16:11,故D错误;
故选C.
点评:本题考查物质的量的计算,为高频考点,把握以物质的量为中心的基本计算公式为解答的关键,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列实验操作中,正确的是( )
| A、为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 |
| B、用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 |
| C、为加速固体物质的溶解只能采用加热的方法 |
| D、为增大气体物质的溶解度,常采取搅拌、加热等措施 |
下列反应的离子方程式正确的是( )
| A、往澄清的石灰水中通入过量CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | ||
B、用小苏打(NaHCO3)治疗胃酸过多:HCO
| ||
C、往碳酸镁中滴加稀盐酸:CO
| ||
D、氢氧化钡溶液与稀H2SO4反应:Ba2++SO
|
下列说法不正确的是( )
| A、煤转化为煤气后燃烧,可以提高燃烧效率 |
| B、在生产、流通和消费等过程中实行“减量化、再利用、资源化” |
| C、化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| D、天然气是气体,它不属于化石燃料 |
下列与有机物结构、性质相关的叙述正确的是( )
| A、在水溶液里,乙酸分子中的-CH3可以电离出H+ |
| B、己烷和苯可以用酸性高锰酸钾溶液鉴别 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和氢气反应生成环己烷的反应类型相同 |
| D、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
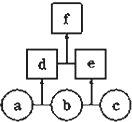 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A、常温下,单质a呈气态 |
| B、单质c具有强氧化性 |
| C、稳定性:d>e |
| D、f受热易分解为d和e |
几种短周期元素的原子半径及主要化合价见下表
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A、单质与稀硫酸反应的速率快慢:R>X>Y |
| B、离子半径:T2->X2+ |
| C、元素最高价氧化物的水化物的碱性:X>R |
| D、单质与氢气化合的难易程度:Z>T |
下列关于粒子结构的描述不正确的是( )
| A、H2S和NH3均是价电子总数为8的非极性分子 |
| B、HS-和HCl均是含一个极性键的18电子粒子 |
| C、CH2C12和CH4均是四面体构型的非极性分子 |
| D、1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值) |
工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.4kJ/mol,下列判断正确的是( )
| A、水煤气反应中生成1mol H2(g)吸收131.4KJ热量 |
| B、CO(g)+H2(g)=C(s)+H2O(l)△H=-131.4kJ/mol |
| C、反应物能量总和大于生成物能量总和 |
| D、水煤气反应中生成1体积CO(g)吸收131.4KJ热量 |