题目内容
4gH2与24.5L(常温常压)CO2相比,所含分子数目多的是 ;各1.5mol上述两种气体相比较,质量大的是 .
考点:物质的量的相关计算
专题:计算题
分析:根据氢气的质量计算氢气的物质的量,相同物质的量时,常温常压下气体的体积大于标准状况下气体的体积;根据物质的量和气体的摩尔质量计算气体的质量.
解答:
解:4gH2的物质的量为
=2mol,
常温常压下气体的摩尔体积大于22.4L/mol,
则24.5L(常温常压)CO2的物质的量<
,
所以,所含分子数目多的是H2,
各1.5mol上述两种气体,m(H2)=1.5mol×2g/mol=3g,
m(CO2)=1.5mol×44g/mol=66g,
所以,各1.5mol上述两种气体相比较,质量大的是CO2,
故答案为:H2;CO2.
| 4g |
| 2g/mol |
常温常压下气体的摩尔体积大于22.4L/mol,
则24.5L(常温常压)CO2的物质的量<
| 24.5L |
| 22.4L/mol |
所以,所含分子数目多的是H2,
各1.5mol上述两种气体,m(H2)=1.5mol×2g/mol=3g,
m(CO2)=1.5mol×44g/mol=66g,
所以,各1.5mol上述两种气体相比较,质量大的是CO2,
故答案为:H2;CO2.
点评:本题考查物质的计算以及气体摩尔体积的应用,题目难度不大,注意物质的量与质量、体积、微粒数目之间的计算公式的运用.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
向0.1mol?L-1 CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起( )
| A、溶液的pH减小 |
| B、CH3COOH的电离程度增大 |
| C、溶液的导电能力减小 |
| D、溶液的c(OH-) 增大 |
有关化学用语的表示正确的是( )
A、甲烷分子的比例模型是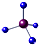 |
B、二氧化碳的电子式: |
C、Cl-的结构示意图为: |
| D、HClO的结构式为H-O-Cl |
下列说法正确的是( )
| A、向NaOH溶液中慢慢滴加FeCl3饱和溶液,可制得Fe(OH)3胶体 |
| B、胶体与其他分散系的本质区别是胶体能发生丁达尔效应 |
| C、除去Fe(OH)3胶体中的Na+和Cl-可用过滤的方法 |
| D、Fe(OH)3胶体中逐滴加入稀硫酸,会产生沉淀而后沉淀溶解 |
对相同质量的SO2和SO3来说,下列关系正确的是( )
| A、含氧原子个数比为2:3 |
| B、含硫元素质量比为4:5 |
| C、含氧元素质量比为5:6 |
| D、含硫原子个数比为1:1 |
下列对于“摩尔”的说法和理解正确的是( )
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、摩尔可以把物质的宏观数量与微观粒子的数量联系起来 |
| C、国际上规定,0.012kg碳原子所含有的碳原子数目为1摩 |
| D、摩尔是物质的量的单位,简称摩,符号为mol |
下列有关说法正确的是( )
| A、若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B、2NO(g)+2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 |
| C、加热0.1 mol?L-1Na2CO3溶液,CO32-的水解程度和溶液的pH均增大 |
| D、由于Ksp(AgCl)>Ksp(AgBr),所以任何情况下AgBr沉淀都不能转化为AgCl沉淀 |