题目内容
12.下列热化学方程式或离子方程式中,正确的是( )| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | Na2CO3溶液呈碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O═2NH4++Mg(OH)2↓ | |
| D. | 氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-++ClO- |
分析 A.甲烷燃烧的热化学方程式中,生成的水应该为液态;
B.碳酸根离子的水解分步进行,主要以第一步为为主;
C.氯化镁与氨水反应生成氢氧化镁沉淀和氯化铵;
D.次氯酸为弱酸,离子方程式中次氯酸不能拆开.
解答 解:A.甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷正确的燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,故A错误;
B.Na2CO3溶液中,碳酸根离子部分水解,溶液呈碱性,碳酸根离子的水解分步正确,主要以第一步为主,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故B错误;
C.氯化镁溶液与氨水反应生成氢氧化镁沉淀,反应的离子方程式为:Mg2++2NH3•H2O═2NH4++Mg(OH)2↓,故C正确;
D.氯气与水反应生成氯化氢和次氯酸,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O?H++Cl-+HClO,故D错误;
故选C.
点评 本题考查离子方程式、热化学方程式的正误判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等,明确热化学方程式的书写原则.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.在0.5molNa2SO4中含有Na+的物质的量为( )
| A. | 2mol | B. | 6.02×1023个 | C. | 0.5mol | D. | 1mol |
3.湿化学法(NPP一法)制备纳米级活性氧化锌,可以用氧化锌粗品(含有FeO、Fe2O3、CuO杂质)为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙烧获得活性氧化锌,其化学工艺流程如下:

已知溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表格:
(1)通过焰色反应可以检验产品中是否含有Na+,该实验的具体操作是将铂丝蘸盐酸在无色火焰上灼烧到无色,再蘸取少量产品在无色火焰上灼烧,观察火焰颜色,若呈黄色,则证明有Na+,反之,则证明没有Na+.
(2)上述流程图中用的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式).加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为:ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
(5)纳米活性氧化锌可用作氯乙烯聚合制取聚氯乙烯的催化剂,写出该反应的化学方程式:nCH2=CHCl$\stackrel{纳米活性氧化锌}{→}$ .
.

已知溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表格:
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.7 | 3.2 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9.0 |
(2)上述流程图中用的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式).加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为:ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
(5)纳米活性氧化锌可用作氯乙烯聚合制取聚氯乙烯的催化剂,写出该反应的化学方程式:nCH2=CHCl$\stackrel{纳米活性氧化锌}{→}$
 .
.
7.下列与金属腐蚀有关的说法正确的是( )
| A. |  图中,插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. |  图中,开关由M改置于N时,Cu-Zn合金的腐蚀速率加快 | |
| C. |  图中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 | |
| D. |  图中,Zn-MnO2干电池为一次性电池,将NH4Cl换成湿的KOH后电池性能更好 |
1.23592U和23892U是铀的两种主要的同位素.U是制造原子弹和核反应堆的主要原料.下列有关说法正确的是( )
| A. | U原子核中含有92个中子 | B. | U原子核外有143个电子 | ||
| C. | 23592U和23892U互为同位素 | D. | 23592U和23892U互为同素异形体 |
2. 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A. | 往平衡体系中加入少量金属铅后,c(Pb2+)增大 | |
| B. | 往平衡体系中加入少量 Sn(NO3)2固体后,c(Pb2+)变小 | |
| C. | 升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 | |
| D. | 25℃时,该反应的平衡常数K=2.2 |
 X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子,G不是稀有气体元素.请回答下列问题:
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子,G不是稀有气体元素.请回答下列问题: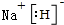 ;ZX与水反应放出气体的化学方程式为2NaH+H2O=2NaOH+H2↑.
;ZX与水反应放出气体的化学方程式为2NaH+H2O=2NaOH+H2↑. Fe+2ZG,放电时,电池的正极反应式为Fe2++2e-=Fe,该电池的电解质为β-Al2O3.
Fe+2ZG,放电时,电池的正极反应式为Fe2++2e-=Fe,该电池的电解质为β-Al2O3.