题目内容
19.一定温度下,在固定容积的密闭容器中发生下列反应:2HI(g)?H2(g)+I2(g).若HI的浓度由0.1mol•L-1降到0.07mol•L-1时需要15s,则HI的浓度由0.07mol•L-1降到0.05mol•L-1时,所需时间为( )| A. | 等于15 s | B. | 等于10 s | C. | 大于10s | D. | 小于10 s |
分析 先根据v=$\frac{△c}{△t}$计算出用HI表示的平均反应速率,然后假设速率不变,根据t=$\frac{△c}{v}$计算出HI的浓度由0.07 mol•L-1降到0.05 mol•L-1时所需反应的时间;最后根据“反应物的浓度减小,反应速率减慢”判断所需时间.
解答 解:15 s内HI的平均反应速率为:v(HI)=$\frac{0.1mol/L-0.07mol/L}{15s}$=0.002 mol•L-1•s-1,
若反应速率不变,HI的浓度由0.07 mol•L-1降到0.05 mol•L-1时所需反应的时间为:$\frac{0.07mol/L-0.05mol/L}{0.002mol/(L•s)}$=10 s,
因反应物浓度越大,反应速率越快,浓度越小,反应速率越慢,则HI的浓度由0.07 mol•L-1降到0.05 mol•L-1时,因反应物的浓度减小,反应速率减慢,则所需时间大于10 s,
故选C.
点评 本题考查浓度对化学反应速率的影响,题目难度不大,明确化学反应速率的概念及表达式为解答关键,注意掌握化学反应速率的影响因素,试题培养了学生的灵活应用能力.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
7.如图中所示的实验方法、装置或操作完全正确的是( )
| A. | 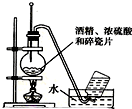 实验室制乙烯 | B. | 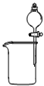 分离苯酚和水 | ||
| C. |  石油的蒸馏 | D. | 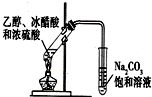 实验室制乙酸乙酯 |
14.已知短周期元素的离子,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径A>B>C>D | B. | 原子序数D>C>B>A | ||
| C. | 离子半径C3->D->B+>A2+ | D. | 单质的还原性A>B>D>C |
4.把质量为 m g的Cu丝灼烧变黑,立即放入下列物质中,使Cu丝变红,而且质量仍为 m g的是( )
| A. | 稀H2SO4 | B. | C2H5OH | C. | 稀HNO3 | D. | CH 3COOH(aq) |
6.通常用来衡量一个国家石油化工发展水平标志的是( )
| A. | 甲烷的产量 | B. | 乙醇的产量 | C. | 乙烯的产量 | D. | 乙酸的产量 |
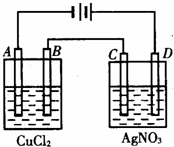 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: