题目内容
某研究性学习小组进行了甲、乙、丙三组实验:各取30 mL相同浓度的NaOH溶液,然后分别缓慢地加入组成相同的硅铝合金粉末,得到下表中有关数据(假设反应前后溶液体积不发生变化,气体体积均在标准状况下测定;已知:Si+2NaOH+H2O====Na2SiO3+2H2实验序号 | 甲 | 乙 | 丙 |
合金质量/g | 0.275 | 0.605 | 0.715 |
气体体积/mL | 392 | 784 | 784 |
请回答下列问题:
(1)甲组实验中,NaOH溶液_________(选填“过量”“适量”或“不足”)。
(2)合金中硅铝的物质的量之比为_________。
(3)计算氢氧化钠溶液的物质的量浓度。
(1)过量 (2)1:1
(3)分析表中数据可知,30 mL NaOH溶液可与0.55 g硅铝合金恰好反应生成784 mLH2。0.55 g硅铝合金中硅和铝的物质的量均为0.01 mol。
根据化学方程式:
Si+2NaOH+H2O====Na2SiO3+2H2![]()
2Al+2NaOH+2H2O====2NaAlO2+3H2![]()
消耗NaOH的物质的量n(NaOH)=0.01 mol×2+0.01 mol=0.03 mol
NaOH溶液的物质的量浓度:
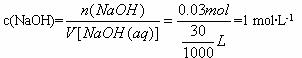

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
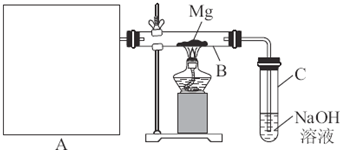

 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).