题目内容
某研究性学习小组进行了如下实验探究:将适量1.00mol?L-1 CuSO4溶液和2.00mol?L-1 NaOH溶液混合,过滤后得到浅绿色碱式盐沉淀A[化学式:aCu(OH)2?CuSO4].将9.08g A隔绝空气在1000℃以上强热,得到了5.76g砖红色固体B(铜的+1价氧化物),同时得到的混合气体C;再将5.76g B溶于稀硫酸得到2.56g另一种红色固体D和蓝色溶液.(已知铜的化合价有+1和+2)(1)实验需用1.00mol?L-1 CuSO4溶液480mL,配制以上溶液需用的玻璃仪器除了烧杯、玻璃棒、量筒外还需
(2)甲同学认为A中含有杂质Na+,除去此杂质的方法是
(3)B与稀硫酸反应的离子方程式为
(4)通过计算确定A的组成为
分析:(1)配制480mL溶液,需要选用500mL容量瓶,根据配制500mL 1.00mol?L-1 CuSO4溶液的步骤选用仪器;
(2)根据n=cV计算出硫酸铜的物质的量,再根据m=nM计算出需要胆矾的质量;
(3)根据钠离子可溶于水中,可以使用水进行洗涤,除去A中的杂质钠离子;
(4)氧化亚铜与稀硫酸反应生成铜和硫酸铜,据此写出反应的离子方程式.
(2)根据n=cV计算出硫酸铜的物质的量,再根据m=nM计算出需要胆矾的质量;
(3)根据钠离子可溶于水中,可以使用水进行洗涤,除去A中的杂质钠离子;
(4)氧化亚铜与稀硫酸反应生成铜和硫酸铜,据此写出反应的离子方程式.
解答:解:(1)实验室没有480mL容量瓶,应该选用500mL的容量瓶,配制该溶液需要的仪器有:烧杯、玻璃棒、胶头滴管、500mL容量瓶等,还缺少500mL容量瓶和胶头滴管;500mL 1.00mol/L的硫酸铜中含有溶质硫酸铜的物质的量为0.5mol,需要胆矾的质量为:250g/mol×0.5mol=125.0g,
故答案为:500ml容量瓶、胶头滴管; 125.0;
(2)向漏斗中加蒸馏水至刚浸没沉淀,让水自然流下,重复此操作2~3次,可以将A中的钠离子除去,
故答案为:向漏斗中加蒸馏水至刚浸没沉淀,让水自然流下,重复此操作2~3次;
(3)氧化亚铜与稀硫酸反应的离子方程式为:Cu2O+2H+=Cu+Cu2++H2O,
故答案为:Cu2O+2H+=Cu+Cu2++H2O;
(4)9.08gA加热得到5.76gCu2O,根据铜元素守恒,9.08gA中含有的铜元素的物质的量为:
×2=0.08mol,则
×(a+1)=0.08mol,解得:a=3,所以A的化学式为:3Cu(OH)2?CuSO4,
故答案为:3Cu(OH)2?CuSO4.
故答案为:500ml容量瓶、胶头滴管; 125.0;
(2)向漏斗中加蒸馏水至刚浸没沉淀,让水自然流下,重复此操作2~3次,可以将A中的钠离子除去,
故答案为:向漏斗中加蒸馏水至刚浸没沉淀,让水自然流下,重复此操作2~3次;
(3)氧化亚铜与稀硫酸反应的离子方程式为:Cu2O+2H+=Cu+Cu2++H2O,
故答案为:Cu2O+2H+=Cu+Cu2++H2O;
(4)9.08gA加热得到5.76gCu2O,根据铜元素守恒,9.08gA中含有的铜元素的物质的量为:
| 5.76g |
| 144g/mol |
| 9.08g |
| (98a+160)g/mol |
故答案为:3Cu(OH)2?CuSO4.
点评:本题考查了复杂化合物化学式的确定、配制一定物质的量浓度的溶液方法、离子方程式的书写等知识点,题目难度中等,注意掌握确定复杂化合物化学式的确定方法,明确配制一定物质的量浓度方法及选用仪器的方法.

练习册系列答案
相关题目

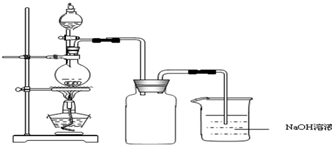 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).