题目内容
11.氟利昂-12的化学式是CCl2F2,下列叙述不正确的是( )| A. | 该分子是平面结构 | B. | 该分子是正四面体型 | ||
| C. | 该分子无同分异构体 | D. | 该物质属于卤代烃 |
分析 该化合物是甲烷的取代产物,属于有机物,甲烷是正四面体型结构,运用知识迁移的方法,与CH4的分子构型对比回答.
解答 解:A.甲烷是正四面体型结构,则氟利昂-12中氯原子、氟原子不同,正四面体结构被压缩,为四面体结构,故A错误;
B.甲烷是正四面体型结构,则氟利昂-12中氯原子、氟原子不同,正四面体结构被压缩,为四面体结构,故B错误;
C.该化合物是甲烷的取代产物,由于甲烷是正四面体型结构,氟利昂-12中氯原子、氟原子不同,正四面体结构被压缩,为四面体结构,因此结构只有一种,没有同分异构体,故C正确;
D.氟里昂-12CCl2F2属于卤代烃,是有机物,故D正确.
故选CD.
点评 本题以甲烷的正四面体型结构为载体,考查学生对知识的迁移和空间想象能力.掌握甲烷正四面体型,乙烯、苯为平面型分子,乙炔为直线型分子.

练习册系列答案
相关题目
1.下列有关化学用语错误的是( )
| A. | 硫离子的核外电子排布式:1s22s22p6 | |
| B. | 碳-14的原子组成符号:${\;}_{6}^{14}$C | |
| C. | 碳原子的外围电子轨道表示式: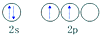 | |
| D. | Cl-的结构示意图: |
19.下列有关混合物的分离与提纯的说法正确的是( )
| A. | 由于碘在乙醇中的溶解度较大,所以可用乙醇把碘水中的碘萃取出来 | |
| B. | 水的沸点为100℃,乙醇的沸点为78.5℃,所以用加热蒸馏的方法使含水乙醇变为无水乙醇 | |
| C. | 由于汽油和水不互溶,因此可用分液的方法将二者分离 | |
| D. | NaCl溶液度随温度下降而减小,所以用冷却法从热的含少量KNO3的NaCl浓溶液中分离得到纯净的NaCl |
6.常温下,将pH=8和pH=10的两强碱溶液等体积混合,则混合溶液的pH为( )
| A. | 8.3 | B. | 9 | C. | 9.7 | D. | 无法确定 |
1.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标况下1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA/22.4 | |
| C. | 1 mol甲基含7 NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
5.钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1.下列说法正确的是( )
| A. | 题述反应条件下还原性:CO>Pd | |
| B. | 题述反应中PdCl2被氧化 | |
| C. | 生成22.4L CO2时,转移的电子为2 mo1 | |
| D. | 题述反应中CO2为还原产物 |
6.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 30g乙烷含有的共价键数目为8NA | |
| B. | 标况下,22.4L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| C. | 1mol甲基含10 NA个电子 | |
| D. | 2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |