题目内容
16.1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式( )| A. | C+H2O═CO+H2 -131.3KJ | B. | C(s)+H2O(g)═CO(g)+H2(g)-10.94KJ | ||
| C. | C(s)+H2O(g)═CO(g)+H2(g)+131.3KJ | D. | C(s)+H2O(g)═CO(g)+H2(g)-131.3KJ |
分析 1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,可知1molC完全反应吸热为12×10.94KJ=131.3KJ,以此来解答.
解答 解:1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,可知1molC完全反应吸热为12×10.94KJ=131.3KJ,则此反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ/mol或C(s)+H2O(g)=CO(g)+H2(g)-131.3KJ,
故选D.
点评 本题考查热化学方程式的书写,为高频考点,把握物质的量与热量的关系、物质的状态、焓变为解答的关键,侧重分析与应用能力的考查,注意热量的表示,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
6. 的一氯代物的种数共有( )
的一氯代物的种数共有( )
 的一氯代物的种数共有( )
的一氯代物的种数共有( )| A. | 3种 | B. | 6种 | C. | 11种 | D. | 12 种 |
7. 在2L密闭容器中,800℃时2NO(g)+O2(g)?2NO2(g)反应体系中,n(NO)随时间的变化如下表:
在2L密闭容器中,800℃时2NO(g)+O2(g)?2NO2(g)反应体系中,n(NO)随时间的变化如下表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第2s时,NO的转化率为60%.
(2)如图所示,表示NO2变化曲线的是b.用O2表示从0--4s内该反应的平均速率v=0.0008mol/(L.s).
(3)当v逆(NO)=2v正(O2)时,该反应是(“是”或“否”)达到平衡状态.
 在2L密闭容器中,800℃时2NO(g)+O2(g)?2NO2(g)反应体系中,n(NO)随时间的变化如下表:
在2L密闭容器中,800℃时2NO(g)+O2(g)?2NO2(g)反应体系中,n(NO)随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,表示NO2变化曲线的是b.用O2表示从0--4s内该反应的平均速率v=0.0008mol/(L.s).
(3)当v逆(NO)=2v正(O2)时,该反应是(“是”或“否”)达到平衡状态.
4.下列说法正确的是( )
| A. | 金属氧化物一定是碱性氧化物 | |
| B. | 胶体和其他分散系的本质区别是分散质粒子大小不同 | |
| C. | 混合物肯定由两种以上元素组成 | |
| D. | 酸性氧化物一定是非金属氧化物 |
11.下列离子方程式书写正确的是( )
| A. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 稀盐酸与苏打溶液反应:HCO3-+H+═CO2↑+H2O | |
| C. | 铁盐腐蚀电路板:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
1.下列叙述正确的是( )
| A. | 根据核磁共振氢谱不能鉴别1-溴丙烷和2-溴丙烷 | |
| B. | 沸点:CH3CH3>CH3CH2OH;密度: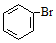 > >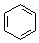 | |
| C. | 苯酚钠溶液中通入少量的CO2离子方程式为:C6H5O-+H2O+CO2→C6H5OH+CO32- | |
| D. | 要检验溴乙烷中的溴元素,向其中加入NaOH溶液共热,冷却后先加硝酸酸化,再加入硝酸银溶液,观察有无浅黄色沉淀生成 |
8. 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )| A. | Y、Z组成的化合物只含离子键 | |
| B. | 氢化物的沸点和稳定性排序:R<Y | |
| C. | 最高价氧化物对应的水化物的酸性:T>R | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定显酸性 |
10.分子式为C12H24O2有机物A,能在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有( )
| A. | 4种 | B. | 16种 | C. | 7种 | D. | 49种 |