题目内容
某化学探究小组用滴定法测定CuSO4?5H2O(Mr=250)含量.取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol/L EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2-=CuY2-+2H+.(EDTA:乙二胺四乙酸白色结晶粉末状固体,呈酸性.)
(1)配制EDTA(H2Y2-)标准溶液时,下列仪器不必要用到的有 (用编号表示).
①电子天平 ②烧杯 ③移液管 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管
(2)写出计算CuSO4?5H2O质量分数的表达式ω= ;
(3)下列操作会导致CuSO4?5H2O含量测定结果偏高的是 .
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除尽可与EDTA反应的干扰离子.
(1)配制EDTA(H2Y2-)标准溶液时,下列仪器不必要用到的有
①电子天平 ②烧杯 ③移液管 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管
(2)写出计算CuSO4?5H2O质量分数的表达式ω=
(3)下列操作会导致CuSO4?5H2O含量测定结果偏高的是
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除尽可与EDTA反应的干扰离子.
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)根据配制一定物质的量浓度的溶液步骤判断使用仪器;
(2)依据滴定实验和反应离子方程式,结合元素守恒计算得到;
(3)滴定实验误差分析依据标准溶液消耗的多少进行分析判断.
(2)依据滴定实验和反应离子方程式,结合元素守恒计算得到;
(3)滴定实验误差分析依据标准溶液消耗的多少进行分析判断.
解答:
解:(1)配制c mol/L EDTA(H2Y2-)标准溶液过程中使用的仪器有:电子天平、容量瓶、玻璃棒、胶头滴管、烧杯,不需要的仪器为:③量筒;
故答案为:③;
(2)滴定反应为:Cu2++H2Y2-=CuY2-+2H+,铜离子物质的量和标准液物质的量相同:cmol/L×b×10-3L=bc×10-3mol;依据元素守恒可得:
20ml溶液中含有的CuSO4?5H2O物质的量为:bc×10-3mol,
则100ml溶液中含硫酸铜晶体的物质的量为:bc×10-3mol×
=5bc×10-3mol,
所以CuSO4?5H2O质量分数的表达式为:
×100%;
故答案为:
×100%;
(3)a.未干燥锥形瓶对实验结果无影响,故a错误;
b.滴定终点时滴定管尖嘴中产生气泡说明消耗标准液读数偏小,结果偏低,故b错误;
c.未除净可与EDTA反应的干扰离子,消耗标准液多,结果偏高,故c正确;
故答案为:C;
故答案为:③;
(2)滴定反应为:Cu2++H2Y2-=CuY2-+2H+,铜离子物质的量和标准液物质的量相同:cmol/L×b×10-3L=bc×10-3mol;依据元素守恒可得:
20ml溶液中含有的CuSO4?5H2O物质的量为:bc×10-3mol,
则100ml溶液中含硫酸铜晶体的物质的量为:bc×10-3mol×
| 100ml |
| 20ml |
所以CuSO4?5H2O质量分数的表达式为:
| cmol/L×b×10-3L×250g/mol×5 |
| ag |
故答案为:
| cmol/L×b×10-3L×250g/mol×5 |
| ag |
(3)a.未干燥锥形瓶对实验结果无影响,故a错误;
b.滴定终点时滴定管尖嘴中产生气泡说明消耗标准液读数偏小,结果偏低,故b错误;
c.未除净可与EDTA反应的干扰离子,消耗标准液多,结果偏高,故c正确;
故答案为:C;
点评:本题通过制备硫酸铜晶体,考查了制备实验方案的设计,试题涉及硫酸铜晶体的制备方法、中和滴定的简单计算和误差的分析,题目难度中等,明确制备原理为解答本题关键,试题充分考查了学生的分析、理解能力及化学实验、化学计算能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是( )
| A、C3N4晶体是分子晶体 |
| B、C3N4晶体中微粒间通过离子键结合 |
| C、C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子 |
| D、C3N4晶体中,C-N键的键长比金刚石中的C-C键的键长要长 |
在月饼盒内常放有一小包干燥剂,该干燥剂的主要成分可能是( )
| A、石灰石 | B、铁屑 |
| C、生石灰 | D、烧碱 |
下列关于元素周期律和元素周期表的说法中正确的是( )
| A、目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 |
| B、元素的性质随着原子序数的增加而呈周期性变化 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、最外层电子数为8的粒子是稀有气体元素的原子 |
可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法正确的是( )
| A、以NaCl溶液或NaOH溶液为电解液时,正极反应式都为:O2+2H2O+4e-═4OH- |
| B、以NaOH溶液为电解液时,负极反应式为Al+3OH--3e-═Al(OH)3 |
| C、以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变 |
| D、电池工作时,电子通过外电路从正极流向负极 |
将氯气通过软管通入鼠洞中,可以用来消灭田鼠.此过程利用了下列哪些氯气的性质( )
①黄绿色 ②密度比空气大 ③有毒 ④易液化 ⑤溶于水.
①黄绿色 ②密度比空气大 ③有毒 ④易液化 ⑤溶于水.
| A、①②③ | B、②③ |
| C、③④ | D、③⑤④ |
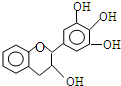 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
| A、分子式为C15H12O5 |
| B、遇FeCl3溶液发生显紫色 |
| C、可以和溴水发生反应 |
| D、1molEGC与4molNaOH恰好完全反应 |

