题目内容
取一定质量的Na2CO3、NaHCO3和Na2SO4的混合物与250 mL,1.00 mol·L-1过量盐酸反应,生成2.016 L CO2(标准状况),然后加入500 mL,0.100 mol·L-1Ba(OH)2溶液,得到沉淀的质量为2.33 g,溶液中过量的碱用、10.0 mL1.00 mol·L-1盐酸恰好完全中和。计算混合物中各物质的质量。
答案:
解析:
解析:
| Na2CO3 7.42g,NaHCO3 l·68g,Na2SO4l.42 g
|

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
(16分)Na2CO3和H2O2结合成棒状晶体,Na2CO3·xH2O2(过氧化氢合相当于水合。注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源…。
现称取一定质量的Na2CO3·xH2O2晶体加热。实验结果以温度和相对质量分数示于下图。
(1)该棒状晶体的化学式Na2CO3·xH2O2中x= 。
(2)加热过程中,在141℃时表现为放热,其原因可能是:
a. Na2CO3·xH2O2分解放热
b.产生的H2O2分解放热
c. Na2CO3·xH2O2分解吸收热量小于产生的H2O2分解放出的热量
(3)事实上,Na2CO3·H2O2(x=1时)是Na2CO4·H2O(Na2CO4叫做过氧碳酸钠)。洗衣粉中加入适 量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。
量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。
(4)写出Na2CO4溶液与稀硫酸反应的离子方程式 。
(5)下列物质不会使过碳酸钠失效的是
| A.MnO2 | B.H2S | C.CH3COOH | D.NaHCO3 |
 。
。 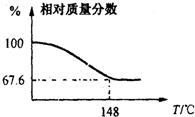 (2012?信阳一模)Na2CO3和H2O2结合成棒状晶体Na2CO3?xH2O2(过氧化氢相当于水合.Na2CO3?xH2O2同时具有Na2CO3和H2O2的性质.注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源.现称取一定质量的Na2CO3?xH2O2晶体加热.实验结果以温度和残留固体的相对质量分数示如图.
(2012?信阳一模)Na2CO3和H2O2结合成棒状晶体Na2CO3?xH2O2(过氧化氢相当于水合.Na2CO3?xH2O2同时具有Na2CO3和H2O2的性质.注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源.现称取一定质量的Na2CO3?xH2O2晶体加热.实验结果以温度和残留固体的相对质量分数示如图. (2012?丹东模拟)为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案:
(2012?丹东模拟)为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案: