题目内容
| |||||||||||||||
答案:
解析:
解析:
(1) |
Mg,Mg+2H2SO4浓===MgSO4+SO2↑+2H2O,C中溶液变红 |
(2) |
2KMnO4+16HCl====2KCl+2MnSO4+5Cl2↑+8H2O,无变化 |
(3) |
浓氨水(或铵盐的浓溶液),酚酞试液,防止倒吸 |

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
某小组同学用下图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
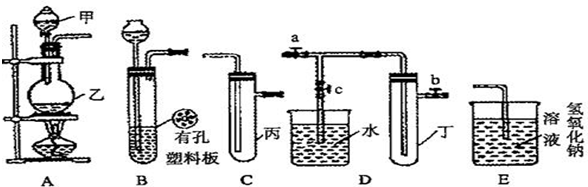
(1)用MnO2和浓盐酸制取氯气,将A、C、E相连,A中反应的离子方程式 .E中氢氧化钠溶液的作用 .
在丙中加入适量水可制得氯水.将所得氯水分成两份,进行实验,其操作、现象、结论为:
①实验I推出的相应结论是否合理? ,若不合理,请说明理由(若合理,无需填写): .
②实验II 推出的相应结论是否合理? ,若不合理,请说明理由(若合理,无需填写): .
(2)为比较Cl2和I2的氧化性强弱,将A、C、E相连,C中盛的试剂可以为 .
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的离子方程式为 .
②若关闭止水夹a、b,打开c,双手紧握(或微热)试管丁,使其中的NO2逸出进入D中,丁中可以观察到的现象 .

(1)用MnO2和浓盐酸制取氯气,将A、C、E相连,A中反应的离子方程式
在丙中加入适量水可制得氯水.将所得氯水分成两份,进行实验,其操作、现象、结论为:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
②实验II 推出的相应结论是否合理?
(2)为比较Cl2和I2的氧化性强弱,将A、C、E相连,C中盛的试剂可以为
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的离子方程式为
②若关闭止水夹a、b,打开c,双手紧握(或微热)试管丁,使其中的NO2逸出进入D中,丁中可以观察到的现象
 完成以下实验:①用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验.在试管I中依次加入2mL 蒸馏水、4mL浓硫酸、2mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管I至微沸状态数分钟后,冷却.
完成以下实验:①用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验.在试管I中依次加入2mL 蒸馏水、4mL浓硫酸、2mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管I至微沸状态数分钟后,冷却.




