题目内容
下列判断正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.C、Si和Ge的最外层电子数都是4,次外层电子数都是8
C.若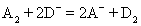 ,则氧化性:A2 > D2
,则氧化性:A2 > D2
D.CO2和SiO2都是酸性氧化物,都不能和氧化钙反应
【答案】
C
【解析】
试题分析:A、硫蒸气能量高,所以等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量多,错误;B、C原子的次外层电子数为2.错误;C、氧化还原反应的氧化性,氧化剂大于氧化产物,所以氧化性:A2 > D2,正确;D、CO2和SiO2是酸性氧化物,CaO为碱性氧化物,酸性氧化物和碱性氧化物反应生成盐,所以CO2、SiO2都可以和CaO反应。
考点:本题考查化学反应的热量变化、电子排布、氧化还原反应。

练习册系列答案
相关题目
在硫酸铁溶液中,加入a g 铜,完全溶解后,又加入b g铁,充分反应后得到c g残余固体,且b<c,则下列判断正确的是( )
| A、最后得到的溶液中不含有Fe3+ | B、残余固体一定全部是铜 | C、最后得到的溶液中只含Cu2+ | D、残余固体可能为铁、铜混合物 |
短周期元素R、T、Q、W、K在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断正确的是( )
| R | ||||
| T | Q | W | K |
| A、含T的盐溶液一定显酸性 |
| B、原子半径及其最高价氧化物对应水化物的酸性:Q<W<K |
| C、最简单气态氢化物沸点和还原性:Q>R |
| D、最简单气态氢化物的热稳定性和水溶液酸性:K>W |
一定条件下,对于可逆反应X(g)+3Y(g)═2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.12mol/L,则下列判断正确的是( )
| A、c1:c2=1:3 | B、平衡时,3VY(正)=2VZ(逆) | C、X、Y的转化率相等 | D、c1的取值范围为0.06<c1<0.16mol/L |