题目内容
下列叙述正确的是
- A.通过沉淀反应,可以使溶液中某种离子的浓度变为0
- B.反应NH3+H3O+=NH4++H2O能自发进行,说明NH3结合H+能力比H2O强
- C.若测得雨水的pH小于7,则下的是酸雨
- D.先将pH试纸用蒸馏水润湿后,再测定溶液的pH
B
试题分析:通过沉淀反应,不可能使溶液中某种离子的浓度变为0,A不正确;pH小于7的雨水不一定是酸雨,酸雨的pH一般小于5.6,C不正确;测定溶液pH的pH试纸不能事先用水润湿,D不正确,答案选B。
考点:考查溶解平衡、反应自发性、酸雨以及溶液pH的测定
点评:该题是基础性试题的考查,试题考查的知识点比较分散,但很基础。试题侧重能力的培养和解题方法的指导,有助于培养学生的逻辑思维能力和发散思维能力,提高学生分析问题、解决问题的能力。
试题分析:通过沉淀反应,不可能使溶液中某种离子的浓度变为0,A不正确;pH小于7的雨水不一定是酸雨,酸雨的pH一般小于5.6,C不正确;测定溶液pH的pH试纸不能事先用水润湿,D不正确,答案选B。
考点:考查溶解平衡、反应自发性、酸雨以及溶液pH的测定
点评:该题是基础性试题的考查,试题考查的知识点比较分散,但很基础。试题侧重能力的培养和解题方法的指导,有助于培养学生的逻辑思维能力和发散思维能力,提高学生分析问题、解决问题的能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
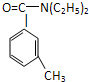 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH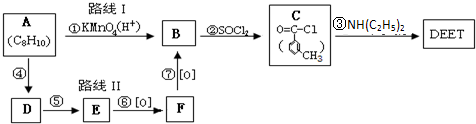
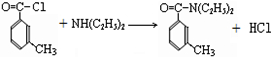
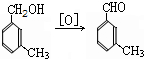
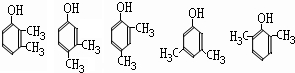 (任写2种)
(任写2种)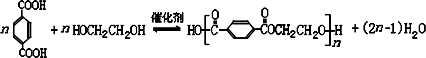
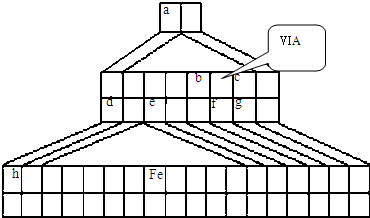
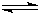 NH3?H2O+H+
NH3?H2O+H+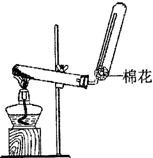 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.