��Ŀ����
15�����ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±�������������ȷ���ǣ�������| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
| ��Ҫ���ϼ� | +2 | +3 | +5��+3��-3 | -2 |
| A�� | XԪ�صĵ��ʳ��������� | |
| B�� | һ�������£�Z������W�ij�������ֱ�ӻ����������������� | |
| C�� | Y������������Ӧ��ˮ����������ϡ��ˮ | |
| D�� | һ�������£�W���ʿ��Խ�Z���ʴ����⻯�����û����� |
���� W���ϼ�Ϊ-2�ۣ�û����������ϼ�+6�ۣ���WΪ��Ԫ�أ�ZԪ�ػ��ϼ�Ϊ+5��+3��-3�����ڢ�A�壬ԭ�Ӱ뾶����Ԫ��������Z����Ԫ�ش���ͬһ���ڣ���ZΪNԪ�أ�X���ϼ�Ϊ+2�ۣ�ӦΪ��A��Ԫ�أ�Y�Ļ��ϼ�Ϊ+3�ۣ����ڢ�A�壬����ԭ�Ӱ뾶����С����֪����λ��ͬһ�����������壬����X��Y��ԭ�Ӱ뾶��W��Zԭ�Ӱ뾶���ܴ���X��YӦ�ڵ������ڣ�����XΪMgԪ�أ�YΪAlԪ�أ�
��� �⣺W���ϼ�Ϊ-2�ۣ�û����������ϼ�+6�ۣ���WΪ��Ԫ�أ�ZԪ�ػ��ϼ�Ϊ+5��+3��-3�����ڢ�A�壬ԭ�Ӱ뾶����Ԫ��������Z����Ԫ�ش���ͬһ���ڣ���ZΪNԪ�أ�X���ϼ�Ϊ+2�ۣ�ӦΪ��A��Ԫ�أ�Y�Ļ��ϼ�Ϊ+3�ۣ����ڢ�A�壬����ԭ�Ӱ뾶����С����֪����λ��ͬһ�����������壬����X��Y��ԭ�Ӱ뾶��W��Zԭ�Ӱ뾶���ܴ���X��YӦ�ڵ������ڣ�����XΪMgԪ�أ�YΪAlԪ�أ�
A��XΪMg�������������Ľ���ΪAl�����ǽ���Mg����A����
B��Z������W�ij�������ֱ�ӻ�������NO��NO�Dz���������������������������B����
C��Y������������Ӧ��ˮ����Ϊ��������������ǿ�ᡢǿ��������ڰ�ˮ����C����
D��һ�������£������백�����Է�Ӧ���ɵ�����ˮ����D��ȷ��
��ѡD��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��Ѷ��еȣ�����Ԫ�صĻ��ϼ���뾶�ƶ�Ԫ���ǽ���Ĺؼ���ע���Ԫ�������ɵ��������գ�

| A�� | ${\;}_{y}^{m}$X | B�� | ${\;}_{y}^{y+m}$X | C�� | ${\;}_{y+n}^{m+y+n}$X | D�� | ${\;}_{y+n}^{y+m-n}$X |
| A�� | �������辧��ķ���ʽ��SiO2 | B�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | ||
| C�� | F-���ӽṹʾ��ͼ�� | D�� | ���Ȼ�̼�ĵ���ʽ��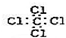 |
| A�� | NH4+��Na+��OH-��SO42- | B�� | NH4+��Mg2+��NO3-��Cl- | ||
| C�� | Ba2+��OH-��Cl-��SO42- | D�� | Fe2+��H+��Cl-��NO3- |
| A�� | C4H10 | B�� | C3H8 | C�� | CH4 | D�� | C2H6 |
| Fe3+ | Cu2+ | Cr3+ | |
| ��ʼ����pH | 2.1 | 4.7 | 4.3 |
| ��ȫ����pH | 3.2 | 6.7 | a |

CaSO4���ܽ��������ͼ�ң���ش��������⣺
��1����ҺI������������Ҫ��Fe2��SO4��3��Cr2��SO4��3��CuSO4���ѧʽ����
��2���ڢڲ������У��ȼ���Ca��OH��2������Һ��pH�����ڷ�ΧΪ3.2��pH��4.3��Ȼ����Һ������80����ȹ��ˣ�����������ijɷ�ΪFe��OH��3��CaSO4��
��3���ڢ۲������У����ֳ�������ש��ɫ�����⣬����������ɫ�̼�����ζ�����壮д���ò����з�����Ӧ�����ӷ���ʽ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��HSO3-+H+=SO2��+H2O
��4��������Ũ�ȡ�1��10-5mol•L-1lʱ��������Ϊ���ӳ�����ȫ���ڢܲ������У���ҪʹCr3+��ȫ����������������Һ��a����СֵΪ5.6������֪Kap[Cr��OH��3]=6.3��10-31��$\root{3}{63}$��4.0��lg4=0.6��
��5��Cr��OH��3���ȷֽ�ΪCr2O3�������ȷ�����ұ����������д�����ȷ������Ļ�ѧ����ʽCr2O3+2Al$\frac{\underline{\;����\;}}{\;}$Al2O3+2Cr��
| A�� | ������������Ŀռ�ṹ | B�� | �����е�̼ԭ���DZ��͵� | ||
| C�� | û��ͬ���칹�� | D�� | �Ǽ����ͬϵ�� |
| A�� | He | B�� | K+ | C�� | Cl- | D�� | Na+ |