题目内容
(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式为 .
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位kJ?mol-1):
根据键能数据计算以下反应的反应热△H,CH4(g)+4F2(g)=CF4(g)+4HF(g)△H= .
(3)已知下列反应在298K时的反应焓变
N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ?mol-1
NH3(g)+HCl(g)=NH4Cl(s)△H=-176.0kJ?mol-1
Cl2(g)+H2(g)=2HCl(g)△H=-184.6kJ?mol-1
反应N2(g)+4H2(g)+Cl2(g)=2NH4Cl(s)在298K时的焓变△H= .
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位kJ?mol-1):
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
(3)已知下列反应在298K时的反应焓变
N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ?mol-1
NH3(g)+HCl(g)=NH4Cl(s)△H=-176.0kJ?mol-1
Cl2(g)+H2(g)=2HCl(g)△H=-184.6kJ?mol-1
反应N2(g)+4H2(g)+Cl2(g)=2NH4Cl(s)在298K时的焓变△H=
考点:热化学方程式,反应热和焓变
专题:化学反应中的能量变化
分析:(1)lg甲烷完全燃烧生成CO2和液态水时放热55.6kJ热量,则16g甲烷燃烧放热889.6KJ,依据热化学方程式书写方法标注聚集状态和对应焓变写出;
(2)依据化学反应的焓变=反应物总键能-生成物总键能计算得到反应的焓变;
(3)根据盖斯定律来解答.
(2)依据化学反应的焓变=反应物总键能-生成物总键能计算得到反应的焓变;
(3)根据盖斯定律来解答.
解答:
解:(1)lg甲烷完全燃烧生成CO2和液态水时放热55.6kJ热量,16g甲烷燃烧放热889.6KJ,依据热化学方程式书写方法标注聚集状态和对应焓变写出热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6 kJ/mol,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6 kJ/mol;
(2)化学反应的焓变=反应物总键能-生成物总键能,
CH4(g)+4F2(g)=CF4(g)+4HF(g)
△H=(414KJ/mol×4+158KJ/mol×4)-(489KJ/mol×4+565KJ/mol×4)=-1928KJ/mol;
故答案为:-1928KJ/mol;
(3)N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ?mol-1 ①
NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ?mol-1②
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ?mol-1③
则由盖斯定律可知,
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)可由①+③+②×2得到,
则△H=△H1+△H3+△H2×2=(-92.2kJ?mol-1)+(-184.6kJ?mol-1)+(-176kJ?mol-1)×2=-628.8kJ/mol,
故答案为:-628.8kJ/mol.
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6 kJ/mol;
(2)化学反应的焓变=反应物总键能-生成物总键能,
CH4(g)+4F2(g)=CF4(g)+4HF(g)
△H=(414KJ/mol×4+158KJ/mol×4)-(489KJ/mol×4+565KJ/mol×4)=-1928KJ/mol;
故答案为:-1928KJ/mol;
(3)N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ?mol-1 ①
NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ?mol-1②
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ?mol-1③
则由盖斯定律可知,
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)可由①+③+②×2得到,
则△H=△H1+△H3+△H2×2=(-92.2kJ?mol-1)+(-184.6kJ?mol-1)+(-176kJ?mol-1)×2=-628.8kJ/mol,
故答案为:-628.8kJ/mol.
点评:本题考查学生燃烧热的热化学方程式的书写和利用盖斯定律来计算反应的反应热,明确已知反应和目标反应的关系是解答本题的关键,难度不大,注重了对高考热点的考查.

练习册系列答案
相关题目
下列说法正确的是( )
| A、16O2和18O2互为同素异形体 |
| B、正丁烷和异丁烷是同系物 |
| C、H和D互为同位素 |
| D、CaF2是含有非极性键的离子化合物 |
如图是产生和收集气体的实验装置,该装置最适合于( )
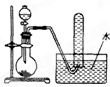

| A、用双氧水与二氧化锰反应制取O2 |
| B、用浓盐酸和MnO2反应制取Cl2 |
| C、用浓氨水和烧碱反应制取NH3 |
| D、用Na2SO3与硫酸反应制取SO2 |
25℃时,相同物质的量浓度下列溶液中,水的电离程度由大到小排列顺序正确的是( )
①KNO3 ②NaOH ③CH3COONH4 ④NH4Cl.
①KNO3 ②NaOH ③CH3COONH4 ④NH4Cl.
| A、③>④>①>② |
| B、④>③>①>② |
| C、③>④>②>① |
| D、①>②>③>④ |
 【化学--选修物质结构与性质】
【化学--选修物质结构与性质】 X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系.回答下列问题:
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系.回答下列问题: