题目内容
已知常温时,物质的量浓度相同的NaX、NaY、NaZ溶液的pH分别为8、9、10,下列说法中不正确的是( )
| A、中和1mol HY酸,需要的NaOH稍小于1mol |
| B、HX、HY、HZ三者均为弱酸 |
| C、在X-、Y-、Z-三者中,Z-最易发生水解 |
| D、在三种酸HX、HY、HZ中以HX酸性相对最强 |
考点:盐类水解的原理
专题:
分析:相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,其相应的酸的酸性越弱,据此解答.
解答:
解:A.这三种酸都是一元酸,一元酸中和氢氧化钠时,酸碱的物质的量相等,所以中和1molHY酸,需要的NaOH等于1mol,故A错误;
B.NaX、NaY、NaZ水溶液都大于7,说明这三种盐都是强碱弱酸盐,所以这三种酸都是弱酸,故B正确;
C.相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,所以Z-水解程度最大,故C正确;
D.相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,其相应的酸的酸性越弱,根据题意知,在三种酸HX、HY、HZ中以HX酸性相对最强,故D正确;
故选A.
B.NaX、NaY、NaZ水溶液都大于7,说明这三种盐都是强碱弱酸盐,所以这三种酸都是弱酸,故B正确;
C.相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,所以Z-水解程度最大,故C正确;
D.相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,其相应的酸的酸性越弱,根据题意知,在三种酸HX、HY、HZ中以HX酸性相对最强,故D正确;
故选A.
点评:本题考查盐类水解,明确酸的强弱与酸根离子水解程度关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中正确的是( )
| A、X、M两种元素只能形成X2M型化合物 |
| B、由于W、Z、M元素的氢化物的相对分子质量依次减小,所以其沸点依次降低 |
| C、元素X、Z、W的单质晶体中含相同类型的化学键 |
| D、元素W和M的某些单质可作为水处理中的消毒剂 |
在2A(g)+B(g)=3C(g)+4D(g)中,表示该反应速率最快的是( )
| A、v(A)=0.5mol?L-1.mim-1 |
| B、v(B)=0.3mol?L-1.mim-1 |
| C、v(C)=0.8mol?L-1.mim-1 |
| D、v(D)=1.0mol?L-1.mim-1 |
铵盐受热易分解,但硝酸铵在不同条件下分解所得产物不同.下列各组物质中可能是硝酸铵分解产物的是( )
| A、O2+HNO3+H2O |
| B、N2+NH3+H2O |
| C、NH3+HNO3 |
| D、NH3+NO+H2 |
海水中蕴含80多种元素,是一个巨大的宝藏,下列有关说法不正确的是( )
| A、锂元素在海水中含量很少,属于微量元素 |
| B、镁用于制造飞机、汽车、火箭,有“国防金属”的美誉 |
| C、从海水中提取物质不一定必须通过化学变化才能实现 |
| D、Mg在CO2中燃烧的反应,CO2既是氧化剂又是还原剂 |
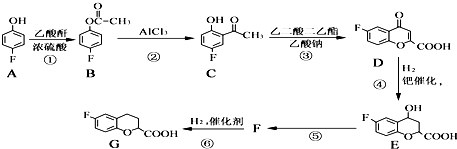
 请回答下列问题:
请回答下列问题: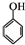 和乙酸酐为原料制备
和乙酸酐为原料制备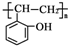 的合成路
的合成路