题目内容
过渡元素高价化合物在酸性条件下有较强的氧化性,如KMnO4、Na2WO4(钨酸钠)等.现向50mL浓度为0.100mol/L的FeCl2溶液中加入25mL浓度为0.0400mol/L的KMnO4,在滴加少量的H2SO4后,两者恰好完全反应.则氧化剂KMnO4的还原产物可能为( )
| A、K2MnO4 |
| B、MnO2 |
| C、MnCl2 |
| D、Mn |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:n(FeCl2)=0.05L×0.1mol/L=0.005mol,反应后被氧化生成Fe3+,Fe元素化合价升高1价,
n(KMnO4)=0.025L×0.04mol/L=0.001mol,根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等计算.
n(KMnO4)=0.025L×0.04mol/L=0.001mol,根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等计算.
解答:
解:n(FeCl2)=0.05L×0.1mol/L=0.005mol,反应后被氧化生成Fe3+,Fe元素化合价升高1价,
n(KMnO4)=0.025L×0.04mol/L=0.001mol,设被还原后Mn元素的化合价为+x,
则0.005mol×(3-2)=0.001mol×(7-x),
x=2,
故选C.
n(KMnO4)=0.025L×0.04mol/L=0.001mol,设被还原后Mn元素的化合价为+x,
则0.005mol×(3-2)=0.001mol×(7-x),
x=2,
故选C.
点评:本题考查氧化还原反应的计算,明确氧化还原反应中元素的化合价升降及电子守恒是解答本题的关键,题目难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
水溶液中能大量共存的一组离子是( )
| A、Na+、Ca2+、Cl-、SO42- |
| B、Fe2+、H+、SO32-、ClO- |
| C、Mg2+、NH4+、Cl-、SO42- |
| D、K+、Fe3+、NO3-、SCN- |
下列说法正确的是( )
| A、分子式为C4H8含碳碳双键的同分异构体(包括顺反异构)共有5种 |
| B、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能,说明有机物分子中的基团间存在相互影响 |
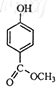
C、芥子醇(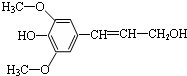 )能发生氧化、取代、水解、加聚反应 )能发生氧化、取代、水解、加聚反应 |
| D、将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成,该物质一定属于醛类 |
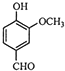
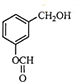
实验室对某有机物有如下实验记录:4位同学据此分别提出以下4种该有机物可能的分子式,其中合理的是( )
①在氧气中完全燃烧,只生成CO2和H2O;
②完全燃烧1mol该有机物需消耗氧气112L(标准状况下).
①在氧气中完全燃烧,只生成CO2和H2O;
②完全燃烧1mol该有机物需消耗氧气112L(标准状况下).
| A、C2H6 |
| B、C4H8O2 |
| C、C3H10O |
| D、C5H10O3 |
下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
| A、K | B、Na | C、Fe | D、Al |
 某类硝酸盐受热分解的产物为不含氮元素的固体物质和NO2、O2气体:
某类硝酸盐受热分解的产物为不含氮元素的固体物质和NO2、O2气体: (1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于
(1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于