��Ŀ����
25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10��5 mol��L-1 | K1��4.4��10-7 mol��L-1 K2=5.6��10-11 mol��L-1�� | 3.0��10��8mol��L-1 |
��ش��������⣺
��1��ͬŨ�ȵ�CH3COO-��HCO3-��CO32-��ClO-���H+��������ǿ������˳��Ϊ________________��
��2��������0.1 mol��L��1��CH3COOH��Һ�ڼ�ˮϡ�����У����б���ʽ������һ����С����________(����ĸ��ţ���ͬ)��
A��c(H��)
B��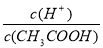
C��c(H��)��c(OH��)
D.
E��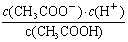
������Һ�����¶ȣ�����5�ֱ���ʽ�������������___________��
��3�����Ϊ10mL pH=2�Ĵ�����Һ��һԪ��HX��Һ�ֱ��ˮϡ����1000mL��ϡ����pH�仯��ͼ����HX�ĵ���ƽ�ⳣ��__________������ڡ��������ڡ���С�ڡ��������ƽ�ⳣ����ϡ�ͺ�HX��Һ����ˮ���������c(H��) __________������ڡ��������ڡ���С�ڡ����������Һ����ˮ���������c(H��)��������______________________________��
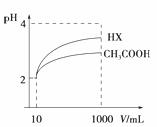
��4����֪100��ʱ��ˮ�����ӻ�Ϊ1��10��12�����¶��²��ij��ҺpH=7������Һ��__________����ᡱ��������С����ԡ������¶���pH=1��H2SO4��ҺaL��pH=11��NaOH��ҺbL��ϣ������û��ҺpH=2����a��b=__________��
һ���¶��£������������Ϊ2.0L�ĵĺ����ܱ������з������·�Ӧ��PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
��� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | �ﵽƽ������ʱ��s�� | |
PCl5��g�� | PCl3��g�� | Cl2��g�� | |||
�� | 320 | 0.40 | 0.10 | 0.10 | t1 |
�� | 320 | 0.80 | t2 | ||
�� | 410 | 0.40 | 0.15 | 0.15 | t3 |
����˵����ȷ����
A��ƽ�ⳣ��K��������>������
B����Ӧ����ƽ��ʱ��PCl5��ת���ʣ�������>������
C����Ӧ����ƽ��ʱ������I�е�ƽ������Ϊv(PCl5)=0.1/t1 mol/(L��s)
D����ʼʱ���������г���PCl5 0.30 mol��PCl3 0.45 mol��Cl2 0.10 mol����Ӧ�����淴Ӧ�� �����
�����


 H����OH�����ڲ�ͬ�¶��������ӻ�ΪKW(25��)��1.0��10��14��KW(35��)��2.1��10��14��������������ȷ����
H����OH�����ڲ�ͬ�¶��������ӻ�ΪKW(25��)��1.0��10��14��KW(35��)��2.1��10��14��������������ȷ����