题目内容
(12分)铝及其化合物用途广泛。工业上焙烧明矾【KAl(SO4)2·12H2O】可得到A12O3,反应的化学方程式为4KAl(SO4)2·12H2O+3S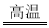 2K2SO4+2A12O3+9SO2↑+48H2O。
2K2SO4+2A12O3+9SO2↑+48H2O。
请回答下列问题:
(1)在焙烧明矾的反应中,被氧化和被还原的元素质量之比是________________。
(2)焙烧明矾时产生的SO2可用来制硫酸。已知25℃、10lkPa时:
①2SO2(g) +O2(g)  2SO3(g) ΔH=—197KJ/mol
2SO3(g) ΔH=—197KJ/mol
②2H2O(g)  2H2O(l)ΔH=—44KJ/mol
2H2O(l)ΔH=—44KJ/mol
③2SO2(g) +O2(g) + 2H2O(g) 2H2SO4(l)ΔH=—545KJ/mol
2H2SO4(l)ΔH=—545KJ/mol
则反应SO3(g)+ H2O(l)= H2SO4(l)ΔH=______KJ/mol。
(3)工业上利用电解熔融的A12O3制备Al,其化学方程式是_____________________;电解时阳极和阴极材料均为石墨,电解时所消耗的电极是__________(填“阳极”或“阴极”)。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式为____________;②电池总反应的化学方程式为________________。
(12分,每空2分)(1)1:2 ;(2)-152;(3)2Al2O3(熔融) 4Al+3O2↑ ;阳极
4Al+3O2↑ ;阳极
(4)①Al+4OH-―3e-=== [Al(OH)4]-;②Al+3NiO(OH)+NaOH+3H2O ===Na[Al(OH)4]+3Ni(OH)2
【解析】
试题分析:(1)在反应S单质中S元素的化合价有反应前单质的0价,变为反应后SO2中的+4价,化合价升高,失去电子,作还原剂,被氧化;4KAl(SO4)2·12H2O+3S 2K2SO4+2A12O3+9SO2↑+48H2O中,KAl(SO4)2·12H2O 中的S元素由反应前的+6价变为反应后SO2中的+4价,化合价降低得到电子,作氧化剂,被还原,所以被氧化和被还原的元素质量之比是3:6=1:2;(2)(③-①-②)÷2,整理可得SO3(g)+ H2O(l)= H2SO4(l)ΔH=-152 KJ/mol;(3) 工业上电解熔融的A12O3制备Al的化学方程式是2Al2O3(熔融)
2K2SO4+2A12O3+9SO2↑+48H2O中,KAl(SO4)2·12H2O 中的S元素由反应前的+6价变为反应后SO2中的+4价,化合价降低得到电子,作氧化剂,被还原,所以被氧化和被还原的元素质量之比是3:6=1:2;(2)(③-①-②)÷2,整理可得SO3(g)+ H2O(l)= H2SO4(l)ΔH=-152 KJ/mol;(3) 工业上电解熔融的A12O3制备Al的化学方程式是2Al2O3(熔融)  4Al+3O2↑;电解时阳极和阴极材料均为石墨,由于石墨是惰性电极,所以电解本身不失去电子而消耗石墨,但是在阳极产生的O2在高温下与C发生反应产生CO2气体而消耗,故电解时所消耗的电极是阳极;(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。①该电池的负极反应式为Al+4OH-―3e-=== [Al(OH)4]-;②电池总反应的化学方程式为Al+3NiO(OH)+NaOH+3H2O ===Na[Al(OH)4]+3Ni(OH)2。
4Al+3O2↑;电解时阳极和阴极材料均为石墨,由于石墨是惰性电极,所以电解本身不失去电子而消耗石墨,但是在阳极产生的O2在高温下与C发生反应产生CO2气体而消耗,故电解时所消耗的电极是阳极;(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。①该电池的负极反应式为Al+4OH-―3e-=== [Al(OH)4]-;②电池总反应的化学方程式为Al+3NiO(OH)+NaOH+3H2O ===Na[Al(OH)4]+3Ni(OH)2。
考点:考查热化学方程式的书写、金属的冶炼原理的方程式表示、物质的消耗、原电池反应的反应原理、氧化还原反应中元素的作用及消耗的质量比的计算的知识。

 阅读快车系列答案
阅读快车系列答案

 Ag
Ag